

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源:不详 题型:单选题
| | 相关实验 | 预期目的 | ||||||
查看答案和解析>> 科目:高中化学 来源:不详 题型:实验题 小军在实验室里做了下列实验: ①分别向盛有稀硫酸和稀盐酸的试管中,滴加紫色石蕊试液;②向盛有稀硫酸的试管中,滴加氢氧化钠试液;③向盛有锌粒的试营中,分别滴加稀盐酸和稀硫酸;④将一根生锈的铁钉分别放入盛有稀盐酸和稀硫酸的试管中,过一会儿取出。 他在纸上记录了以下现象: a. 溶液没有明显现象;b. 溶液变为黄色;c. 溶液显红色;d. 产生气泡,溶液无色。 下面请你来整理完成实验报告。 (1)实验目的:探究__________(填写物质类别)的化学性质。 (2)实验现象:产生a现象的实验所对应的一类反应通常被我们称作__________反应(该反应属于复分解反应)。 (3)上题所涉及的这类反应在日常生活和工农业生产中有广泛的应用。请举出一个利用该反应的实例:______________________________。 查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 以下实验或操作不能达到目的的是
查看答案和解析>> 科目:高中化学 来源:不详 题型:计算题 请根据下列实验数据确定某水合物含Fe2+的盐的化学式。 (1)将0.784 g该含亚铁的盐强烈加热至质量恒定,得到0.160 g Fe2O3; (2)将0.784 g该盐溶于水,加入过量的BaCl2溶液,得到0.932 g BaSO4; (3)0.392 g该盐溶于水,加入过量的NaOH溶液后煮沸,释放出的氨气用50.0 mL 0.10 mol·L-1盐酸吸收后,吸收液需要30.0 mL 0.10 mol·L-1NaOH溶液恰好中和。 查看答案和解析>> 科目:高中化学 来源:不详 题型:实验题 现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置确定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水) 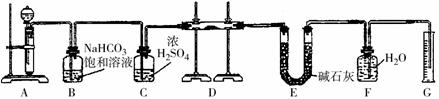  回答下列问题: (1)实验前必须检查装置的气密性。仪器连接好后,在 中加适量的水,关闭A中分液漏斗阀门后微热试管,若看到 说明装置气密性好。 (2)装置A中液体试剂选用盐酸而不用硫酸,理由是 。 (3)装置B的作用是 ; 装置C的作用是 ; 装置E中碱石灰的作用是 。 (4)装置D中发生反应的化学方程式是: 。 (5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为 。 查看答案和解析>> 科目:高中化学 来源:不详 题型:实验题 某同学为了探究硫与氧气的反应情况,装配好如图所示得装置,待内外空气压强不变时标注出水银液面的刻度(用红漆)。取下橡皮塞,在玻璃燃烧匙中加入硫粉,用酒精灯点燃迅速移入锥形瓶中并塞紧橡皮塞。硫粉安静地燃烧,水银柱推向左管。当火焰熄灭后,静置,水银柱又慢慢地回到原先标定的刻度。简要回答下列问题: 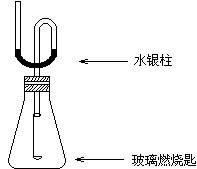 (1)水银柱推向左管说明什么? _______________________________________________。 (2)硫粉未燃尽时火焰就熄灭了,说明_________________________________。 (3)根据水银柱最后又回到原先标定的刻度,可得到什么结论? __________________________________________________________________。 (4)根据反应方程式S + O2 ="=" SO2和上述结论又可推导出什么?(或证明什么?) _______________________________________________________________________。 查看答案和解析>> 科目:高中化学 来源:不详 题型:实验题  某研究性小组借助A-D的仪器装置完成有关实验 某研究性小组借助A-D的仪器装置完成有关实验   【实验一】收集NO气体。 【实验一】收集NO气体。(1)  用装置A收集NO气体,正确的操作上 (填序号)。 用装置A收集NO气体,正确的操作上 (填序号)。 a.从①口进气,用排水法集气 b.从①口进气,用排气法集气 a.从①口进气,用排水法集气 b.从①口进气,用排气法集气 c.从②口进气,用排水法集气 d..从②口进气,用排气法集气 c.从②口进气,用排水法集气 d..从②口进气,用排气法集气 【实验二】为了探究镀锌薄铁板上的锌的质量分数 【实验二】为了探究镀锌薄铁板上的锌的质量分数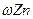 和镀层厚度,查询得知锌易溶于碱:Zn+2NaOH=Na2ZnO3+H2↑据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1 g。用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验。 和镀层厚度,查询得知锌易溶于碱:Zn+2NaOH=Na2ZnO3+H2↑据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1 g。用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验。 方案甲:通过测量试样与碱反应生成的氢气体积来实现探究木目标。 方案甲:通过测量试样与碱反应生成的氢气体积来实现探究木目标。 (2)选用B和 (填仪器标号)两个装置进行实验。 (2)选用B和 (填仪器标号)两个装置进行实验。 (3)测得充分反应后生成氢气的体积为VL(标准状况), (3)测得充分反应后生成氢气的体积为VL(标准状况),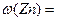 = 。 = 。 (4)计算镀层厚度,还需要检索的一个物理量是 。 (4)计算镀层厚度,还需要检索的一个物理量是 。 (5)若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将(填“偏大”、“偏小”或“无影响”)。 (5)若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将(填“偏大”、“偏小”或“无影响”)。 方案乙:通过称量试样与碱反应前后的质量实现探究目标。选用仪器C做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2g 。 方案乙:通过称量试样与碱反应前后的质量实现探究目标。选用仪器C做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2g 。 (6) (6)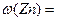 。 。 方案丙:通过称量试样与碱反应前后仪器、试样和试剂的总质量(其差值即为H2的质量)实现探究目标。实验同样使用仪器C。 方案丙:通过称量试样与碱反应前后仪器、试样和试剂的总质量(其差值即为H2的质量)实现探究目标。实验同样使用仪器C。 (7)从实验误差角度分析,方案丙 方案乙(填“优于”、“劣于”或“等同于”)。 (7)从实验误差角度分析,方案丙 方案乙(填“优于”、“劣于”或“等同于”)。查看答案和解析>> 科目:高中化学 来源:不详 题型:问答题 为了降低电子垃圾对环境构成的影响,将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线: 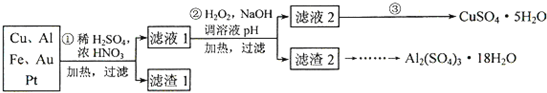 (1)第①步Cu与混酸反应的离子方程式为______.得到滤渣1的主要成分为______. (2)第②步中加入H2O2的作用是______,使用H2O2的优点是______;调溶液pH的目的是______. (3)简述第③步由滤液2得到CuSO4?5H2O的方法是______. (4)由滤渣2制取Al2(SO4)3?18H2O,设计了以下三种方案: 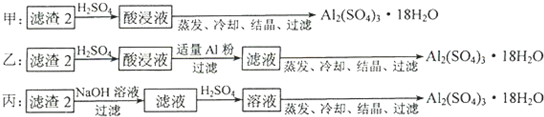 上述三种方案中,______方案不可行,原因是______;从原子利用率角度考虑,______方案更合理. (5)用滴定法测定CuSO4?5H2O含量.取ag试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用 cmol/LEDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液bmL.滴定反应如下: Cu2++H2Y2-→CuY2-+2H+.写出计算CuSO4?5H2O质量分数的表达式ω=______. 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |