
【题目】(1).将HI(g)置于密闭容器中,某温度下发生下列变化:2HI(g) ![]() H2(g)+I2(g) △H<0
H2(g)+I2(g) △H<0
①该反应平衡常数的表达式为K=__________。
②当反应达到平衡时c(I2)=0.5mol/L,c(HI)=4mol/L,则c(H2)为________,HI的分解率为_________。
(2)在一定条件下,A气体与B气体反应生成C气体,反应过程中,反应物与生成物的浓度随时间变化的曲线如图,则
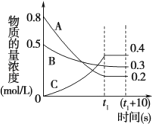
①该反应的化学方程式为:______________
②t1 s时反应物A的转化率为:__________
③0~t1 s内A的反应速率为v(A)=______。
【答案】![]() 0.5mol/L 20% 3A+B
0.5mol/L 20% 3A+B![]() 2C 75%
2C 75% ![]() mol/(L
mol/(L![]() s)
s)
【解析】
(1)①化学平衡常数=![]() ,据此进行解答;②据化学方程式可知,生成0.5mol碘单质分解了1molHI,反应开始前HI浓度为5mol/L,分解率=
,据此进行解答;②据化学方程式可知,生成0.5mol碘单质分解了1molHI,反应开始前HI浓度为5mol/L,分解率=![]() ×100%;
×100%;
(2)①由图象可知,在反应中,A、B的浓度逐渐减小,C的浓度逐渐增大,则A、B为反应物,C为生成物,t1s时A、B浓度不变且不为0,说明是可逆反应,化学反应中浓度变化之比等于化学计量数之比,进而书写反应方程式;
②t1s时反应物A的浓度变化量为(0.8-0.2)mol/L=0.6mol/L,A的转化率=![]() ×100%;
×100%;
③0~t1s内A的浓度变化量为(0.8-0.2)mol/L=0.6mol/L,根据v=![]() 计算v(A)。
计算v(A)。
(1) ①反应2HI(g)H2(g)+I2(g)的平衡常数表达式为:K=![]() =
= ![]() ,故答案为:
,故答案为:![]() ; ②当反应达到平衡时c(I2)=0.5mol/L,c(HI)=4mol/L,根据反应2HI(g)H2(g)+I2(g)可知,平衡时c(H2)=c(I2)=0.5mol/L,反应消耗HI的浓度为:c(HI)消耗=2c(H2)═1mol/L,则反应前HI的总浓度为:4mol/L+1mol/L=5mol/L,所以HI的分解率=
; ②当反应达到平衡时c(I2)=0.5mol/L,c(HI)=4mol/L,根据反应2HI(g)H2(g)+I2(g)可知,平衡时c(H2)=c(I2)=0.5mol/L,反应消耗HI的浓度为:c(HI)消耗=2c(H2)═1mol/L,则反应前HI的总浓度为:4mol/L+1mol/L=5mol/L,所以HI的分解率=![]() ×100%=
×100%=![]() ×100%=20%,故答案为:0.5mol/L;20%;
×100%=20%,故答案为:0.5mol/L;20%;
(2)①由图象可知,在反应中,A、B的浓度逐渐减小,C的浓度逐渐增大,则A、B为反应物,C为生成物,t1s时A、B浓度不变且不为0,说明是可逆反应,t1s内△c(A):△c(B):△c(C)=(0.8-0.2):(0.5-0.3):0.4=3:1:2,化学反应中浓度变化之比等于化学计量数之比,则化学方程式为3A+B![]() 2C,故答案为:3A+B
2C,故答案为:3A+B![]() 2C;
2C;
②t1s时反应物A的浓度变化量为(0.8-0.2)mol/L=0.6mol/L,A的转化率=![]() ×100%=
×100%=![]() ×100%=75%,故答案为:75%;
×100%=75%,故答案为:75%;
③0~t1s内A的浓度变化量为(0.8-0.2)mol/L=0.6mol/L,则v(A)=![]() =
=![]() mol/(L
mol/(L![]() s),故答案为:
s),故答案为:![]() mol/(L
mol/(L![]() s)。
s)。


科目:高中化学 来源: 题型:
【题目】以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OH![]() ClO+Cl+H2O是放热反应。
ClO+Cl+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
(2)步骤Ⅱ合成N2H4·H2O的装置如题19图1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。

(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、![]() 、
、![]() 随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。
随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。

①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,合理的是( )。

A. 图①:验证H2CO3酸性强于H2SiO3 B. 图②:收集CO2或NH3
C. 图③:分离Na2CO3溶液与CH3COOC2H5 D. 图④:分离C2H5OH与CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物的叙述不正确的是___。
A.Li2SO4难溶于水
B.Li与N2反应产物是Li3N
C.LiOH难溶于水
D.LiOH与Li2CO3受热都易分解
(2)与铝位于对角线位置的第二周期元素是Be,能区别Be(OH)2和Mg(OH)2的一种试剂是___,反应的离子方程式为___。
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。它在周期表中的位置是___。
(4)关于与镓同主族的第六周期元素性质的推测中不正确的是___。
A.单质是银白色较软的金属
B.其氢氧化物是两性氢氧化物
C.在化合物中显+3价
D.单质与盐酸的反应比铝剧烈
(5)写出短周期主族元素中原子半径最大的原子的单质在空气中加热条件下反应产物的电子式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下用过量铁块与稀硫酸反应制取氢气,采取下列措施:①将铁块换为等质量的铁粉;②加入少量![]() 溶液;③加入少量
溶液;③加入少量![]() 固体;④加入少量水;⑤加热⑥将稀硫酸换为
固体;④加入少量水;⑤加热⑥将稀硫酸换为![]() 的硫酸,其中可提高
的硫酸,其中可提高![]() 的生成速率的措施有
的生成速率的措施有
A.①③④B.①③⑤C.②④⑤D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A. 由图甲知,B点SO2的平衡浓度为0.3mol·L-1
B. 由图甲知,A点对应温度下的平衡常数为80
C. 达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示
D. 压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制取硫酸中的一步重要反应是![]() 在
在![]() 下催化氧化:
下催化氧化:![]() ,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法错误的是
,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法错误的是
A.达到平衡时,![]() 的浓度与
的浓度与![]() 的浓度相等
的浓度相等
B.若消耗![]() 同时生成
同时生成![]() ,则反应达到平衡
,则反应达到平衡
C.在上述条件下,![]() 不可能
不可能![]() 地转化为
地转化为![]()
D.使用催化剂是为了加快反应速率,提高生产效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如图:

(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的离子方程式是_________________。
(2)过程Ⅰ中,Fe2+催化过程可表示为:
ⅰ:2Fe2++PbO2+4H++SO![]() ===2Fe3++PbSO4+2H2O
===2Fe3++PbSO4+2H2O
ⅱ:……
①写出ⅱ的离子方程式:_______________________________________。
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b._________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com