
【题目】下列方程式书写不正确的是( )
A. 乙烯使溴的四氯化碳溶液褪色:Br2+CH2=CH2→CH2BrCH2Br
B. 用惰性电极电解硝酸锌溶液:2Zn2++2H2O![]() 2Zn+O2↑+4H+
2Zn+O2↑+4H+
C. 实验室制乙炔:CaC2+2H2O →C2H2↑+Ca(OH)2
D. 溴乙酸与氢氧化钠溶液共热:BrCH2COOH+OH—![]() BrCH2COO—+H2O
BrCH2COO—+H2O
科目:高中化学 来源: 题型:
【题目】室温下,下列指定溶液中微粒的浓度关系正确的是( )
A. ![]() 溶液中:
溶液中:![]()
B. ![]() 溶液中:
溶液中:![]()
C. ![]() 弱酸
弱酸![]() 与
与![]() 溶液等体积混合的溶液中:
溶液等体积混合的溶液中: ![]()
D. ![]() 溶液与同浓度等体积盐酸混合的溶液中:
溶液与同浓度等体积盐酸混合的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物。回答下列问题:
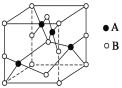
(1)写出基态Cu+的核外电子排布式:______;C、N、O三种元素的第一电离能由大到小的顺序是______
(2)如图是铜的某种氧化物的晶胞示意图,该氧化物的化学式为__________。
(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,在滴加氨水至沉淀刚好全部溶解时可得到蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀。该深蓝色沉淀中的NH3通过___键与中心离子Cu2+结合;NH3分子中N原子的杂化方式是____与NH3分子互为等电子体的一种微粒是________(任写一种)。
(4)CuO的熔点比CuCl的熔点________(填“高”或“低”)。
(5)CuO在高温下易转化为Cu2O,其原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶液中可能存在Na+、Al3+、Fe2+、NH4+、NO3-、CO32-、SO42-中的几种离子,且存在的各离子具有相同的物质的量,某同学对该溶液进行如下实验:
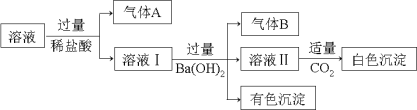
下列判断正确的是
A.气体A一定是CO2,气体B一定是NH3
B.白色沉淀不可能是Al(OH)3
C.溶液中一定存在Al3+、Fe2+、NO3-、NH4+
D.溶液中一定不存在大量Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定Cl2、Br2的氧化性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)。实验步骤如图,填写图中的空白。
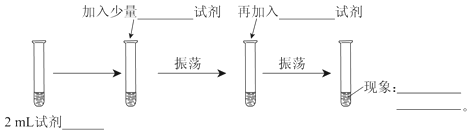
(1)2mL试剂___;
(2)加入少量___试剂;
(3)再加入___试剂;
(4)现象___。
(5)可以证明Cl2的氧化性___(填强于、弱于)Br2的氧化性。
(6)发生反应的离子反应方程式为___。
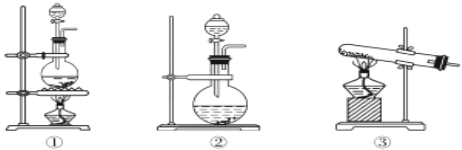
(7)实验室制取氯气用下面装置___(用①②③填写),试着写出制取氯气的反应方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表所列的是五种短周期元素的原子半径及主要化合价(已知铍的原子半径为0.089nm)。
元素代号 | A | B | C | D | E |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
(1)比较A、B、E三种元素的简单离子的离子半径大小___(用对应元素离子符号表示)。
(2)A元素简单离子的结构示意图为__,B元素位于周期表中第__周期__族。
(3)B的最高价氧化物对应水化物与C的最高价氧化物对应水化物反应的离子方程式为__。
(4)上述五种元素的最高价氧化物对应水化物中酸性最强的是__(填化学式)。
(5)C、E形成的化合物为__(填化学式)。
(6)用电子式表示A和D形成化合物的过程___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,探究铜与稀HNO3的反应过程如图:
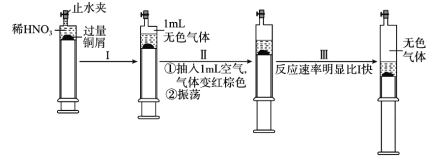
下列说法不正确的是( )
A.过程I中生成无色气体的离子方程式是3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
B.步骤III反应速率比I快的原因是NO2溶于水,使c(HNO3)增大
C.由实验可知,NO2对该反应具有催化作用
D.当活塞不再移动时,打开止水夹,滴加稀硫酸,铜可以继续溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组经查阅资料得知常温下过量的氨气和氯气能反应生成氯化铵,该实验小组对该反应进行探究,部分实验装置如下(夹持装置略去)
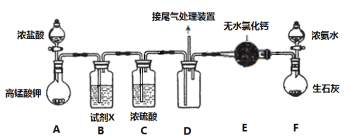
回答下列问题
(1)装置F是NH3的制备装置,其中盛放浓氨水的仪器名称是___________,再写出一种在实验室制备NH3的反应原理(用化学方程式表示)____________。
(2)某同学认为应将E中的无水氯化钙换成碱石灰,他的理由______________。
(3)装置A中发生反应的离子方程式为___________。
(4)装置B中盛装的试剂X的名称为_________,该装置的作用为__________。
(5)装置D的设计中有明显不足之处,请提出改进意见______________。
(6)某同学设计实验证明装置D中所得固体为氯化铵,请把实验步骤写完整:
①取少量装置D中所得固体产物配成溶液,并取少量溶液于两支试管中;
②__________________________;
③向另一只试管中加过量稀硝酸,再加AgNO3溶液,有白色沉淀生成,结论:常温下过量的氨气和氯气反应可生成氯化铵。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com