
����Ŀ��ʵ����������480mL0.2mol��L-1��NaOH��Һ��
(1)ͨ�������֪��Ӧ��������ƽ����_____��NaOH���塣
(2)��ʵ������Ҫ�IJ�����������Ͳ����ͷ�ιܡ��ձ����_____��
(3)������ѡ������IJ�����д����ȷ��˳��_____������ĸ����
A.ϴ�� B.��ȴ C.��ȡ D.���� E.���� F.ת����Һ G.ϡ�� H.�ܽ�
(4)��ʵ������г������������������Һ��Ũ���к�Ӱ��(����ƫ��������ƫ����������Ӱ����)��
�ٶ���ʱ������ˮ���������˿̶�_____��
������ƿ�������һ����ˮ��_____��
�۶���ʱ���ӹ۲쵽Һ��պõ���̶���_____��
(5)��NaOH��Һ��2.24L����(STP)��ǡ����ȫ��Ӧ��������������Һ_____mL��
(6)��18mol��L-1����������100mL1.0 mol��L-1���ᣬʵ��ʱӦѡ�õ�������_____�����ţ���
A.100mL��Ͳ B.������ƽ C.������ D.50mL����ƿ
E.10mL��Ͳ F.��ͷ�ι� G.50mL�ձ� H.100mL����ƿ
���𰸡�4.0 500mL ����ƿ DHBFAE ƫ�� ��Ӱ�� ƫ�� 1000 CEFGH
��������
(1)����ʵ������ѡ�����ѡ��500mL����ƿ������Һ������c=![]() ��m=nM�������ʵ�������
��m=nM�������ʵ�������
(2)����������Һ�IJ������ʹ�õĸ���������
(3)����������Һ�IJ���������
(4)�������ʵ���Ũ�ȶ���ʽc=![]() ����ʵ����
����ʵ����
(5)����������NaOH��Ӧ�����ʵ�����ϵ���ȼ�����ҪNaOH�����ʵ�����Ȼ�����n=cV���㣻
(6)������������ΪҺ̬���ʼ��������ʵ���Ũ����Һ�IJ�������ȷ��ʹ�õ�������
(1)ѡ��500mL����ƿ������Һ����c=![]() ��֪n=c��V=0.2mol/L��0.5L=0.1mol������Ҫ���������ʵ�����m=nM=0.1mol��40g/mol=4.0g��
��֪n=c��V=0.2mol/L��0.5L=0.1mol������Ҫ���������ʵ�����m=nM=0.1mol��40g/mol=4.0g��
(2)����һ�����һ�����ʵ���Ũ�ȵ���Һ��������Ҫ�IJ�����������Ͳ����ͷ�ιܡ��ձ��Ҫ��һ����������ƿ����ʵ����û��480mL������ƿ������ѡ�������ı��������ԭ��Ҫʹ��500mL������ƿ��
(3)ȷ����һ�����һ�����ʵ���Ũ�ȵ���Һ�IJ����Ǽ��㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȣ����Ժ���˳��ΪD��H��B��F��A��E��
A.ϴ�� B.��ȴ C.��ȡ D.���� E.���� F.ת����Һ G.ϡ�� H.�ܽ⣻
(4)�ٶ���ʱ������ˮ���������˿̶ȣ�ʹVƫ�����������ʵ����ʵ������䣬���������Һ��Ũ��ƫ�ͣ�
������ƿ�������һ����ˮ�֣���Ӱ�����ʵ���������Һ���������˶�������Һ��Ũ����Ӱ�죻
�۶���ʱ���ӹ۲쵽Һ��պõ���̶��ߣ���ʹ��Һ�����ƫ�������Ƶ���ҺŨ��ƫ�ͣ�
(5)Cl2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ��Cl2+2NaOH=NaCl+NaClO+H2O��n(Cl2)=2.24L��22.4L/mol=0.1mol������ݷ���ʽ�����ʷ�Ӧ���Ĺ�ϵ��֪��NaOH�����ʵ���Ϊ0.2mol������n=cV��֪���NaOH��Һ�����V=0.2mol��0.2mol/L=1L=1000mL��
(6) 100mL1.0 mol/L��������ʵ���n(H2SO4)=1.0mol/L��0.1L=0.1mol��������Һ��ϡ��ǰ�����ʵ����ʵ������䣬������18mol/L��Ũ��������V=0.1mol��18mol��L-1=0.0056L=5.6mL��Ũ�����Һ̬������Ҫʹ��10mL����Ͳ��ȡ����ʹ��100mL����Ͳ��������ƽ������ȡ��Ũ����ת����ʢ��һ����ˮ��50mL���ձ��У��ò��������裬ʹ�ܽ�ų�������Ѹ����ɢ����ȴ��ͨ������������ת����100mL������ƿ�У�Ȼ��������ˮϴ���ձ�����������ϴ��ҺҲת��������ƿ�У��ټ�ˮ��Һ����̶���1-2cm�������ý�ͷ�ιܵμ�����Һ����̶������У�ҡ�Ⱦ͵õ�100mL1.0 mol.L���ᣬ��ʹ�õ�������10mL��Ͳ��50mL�ձ�������ƿ��100mL����ƿ����ͷ�ιܣ�����ѡ�������CEFGH��


 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺
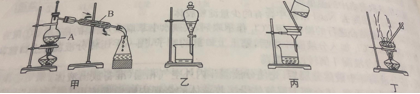
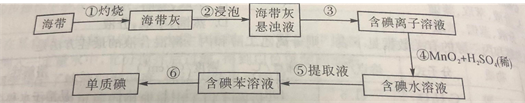
��1��Ϊ�˴Ӻ�������ȡ�⣬ij�о���ѧϰС����Ʋ�����������ʵ�飺
a.���պ���ʱ������Ҫ���ż��⣬����Ҫ�õ�ʵ��������_____������ĸ����
A.�ձ� B.���� C.������ D.������ E.�ƾ��� F.������
b.����۵�ʵ��ѡ������ͼ_____����ס����ҡ�������װ�á�����ݵ�ʵ�����������_____��ѡ������ͼ_____����ס����ҡ�������װ�á������Ŀ���ǴӺ��ⱽ��Һ�з�������ӵ⣬ͬʱ���ձ����ò����ʵ�����������_____��ѡ������ͼ_____����ס����ҡ�������װ�á�
��2��ij�εĻ����Һ�к���Na+��Mg2+��Cl-��SO42-���ӣ����Na+��Mg2+ ��Cl-�����ʵ���Ũ������Ϊ0.2molL-1��0.25molL-1��0.4molL-1����c(SO42-)=_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ѧԺ�����Ŷ��о��������ڳ��³�ѹ�Ϳɼ����£�����LDH��һ�ֹ���������ϳ�NH3��ԭ��ʾ��ͼ���ҡ�����˵������ȷ����

A. �ù��̽�̫����ת����Ϊ��ѧ��
B. �ù����У�ֻ�漰���Լ��Ķ���������
C. �������뻹ԭ�������ʵ���֮��Ϊ1��3
D. ԭ����N2��ͨ������Һ̬�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��ݵ��ܱ������У�ij���ⷴӦ��MHx(s)+yH2(g)![]() MHx+2y(s) ��H<0�ﵽ��ѧƽ�⡣�����й�������ȷ���ǣ� ��
MHx+2y(s) ��H<0�ﵽ��ѧƽ�⡣�����й�������ȷ���ǣ� ��
A. �����£��÷�Ӧ��ƽ�ⳣ����С
B. ����y mol H2ֻ��1 mol MHx
C. �����������ܶȱ��ֲ���
D. ����������ͨ��������������v(����)>v(����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaOH��Na2CO3�����Һ�еμ�0.1 mol��L1ϡ���ᣬCO2����������������������Ĺ�ϵ��ͼ�������ж���ȷ����
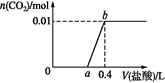
A. ��0~a��Χ�ڣ�ֻ�����кͷ�Ӧ
B. ab�η�����Ӧ�����ӷ���ʽΪ��![]()
C. a=0.3
D. ԭ�����Һ��NaOH��Na2CO3�����ʵ���֮��Ϊ1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������̼����(Na2CS3)������ɱ��������������ijС�����ʵ��̽�������̼���Ƶ����ʲ��ⶨ����Һ��Ũ�ȡ�
ʵ��1��̽��Na2CS3������
���� | ���������� |
�� | ȡ����Na2CS3 ������������ˮ���Ƴ���Һ���ֳ����ȷ� |
�� | ������һ����Һ�еμӼ��η�̪��Һ����Һ���ɫ |
�� | ����һ����Һ�еμ�����KMnO4��Һ����ɫ��ȥ |
��1��H2CS3��________�ᣨ����ǿ��������������
��2����֪����۵�����������SO42����д���÷�Ӧ�����ӷ���ʽ________________________��
ʵ��2���ⶨNa2CS3��Һ��Ũ�ȣ�����ͼ��ʾ���Ӻ�װ�ã�ȡ100mLNa2CS3��Һ����������ƿ�У�������d�Ļ�������������2.0mol/LϡH2SO4���رջ�����
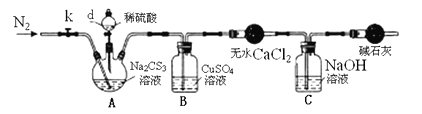
��֪��Na2CS3 + H2SO4=Na2SO4 + CS2 + H2S����CS2��H2S���ж���CS2������ˮ���е�46�棬��CO2ijЩ�������ƣ���NaOH��������Na2COS2��H2O��
��3��ʢ����ˮCaCl2��������������____________��
��4����Ӧ���������k���ٻ���ͨ����N2һ��ʱ�䣬��Ŀ����___________________��
��5��Ϊ�˼���Na2CS3��Һ��Ũ�ȣ���B�л������й��ˡ�ϴ�ӡ�������أ���19.2g���壬��A��Na2CS3�����ʵ���Ũ��Ϊ____________________��
��6����������ʵ�鷽����������ͨ���ⶨC����Һ����������ֵ������Na2CS3��Һ��Ũ�ȣ�����Ӧ������ͨ��N2��Ϊͨ�ȿ���������ֵ________������ƫ��������ƫ����������Ӱ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ����������ӣ�H+��Mg2+��Al3+��NH4+��Cl����AlO2-���������Һ����μ���NaOH��Һʱ���������������ʵ���(n)�����NaOH��Һ�����(V)�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��

A. ԭ��Һ��һ�����е���������H+��Mg2+��Al3+��NH4+
B. ��Ӧ����γɵ���Һ�е����ʺ�AlCl3
C. ԭ��Һ��Al3+��NH�����ʵ���֮��Ϊ1��3
D. ԭ��Һ�к��е���������Cl����AlO2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ȤС���ijƷ�������е�Ħ�����ɷּ��京����������̽����������ϣ�������Ħ������̼��ơ�����������ɣ������������ɷ���������ʱ�����������
��Ħ���������������Ķ��Լ���
ȡ����������Ʒ����ˮ������衢���ˡ�
��1���������м������ NaOH��Һ�����ˡ�����������NaOH��Һ��Ӧ�����ӷ���ʽ��_________________��
��2������1��������Һ����ͨ�����������̼���ټ������ϡ���ᣬ�۲쵽��������__________________��ͨ�����������̼�����ӷ���ʽ��_________________��
��������Ʒ��̼��ƵĶ����ⶨ
������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨC�����ɵ�BaCO3������������ȷ��̼��Ƶ�����������
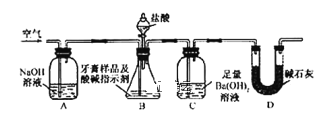
����ʵ����̻ش��������⣺
��3��ʵ����������������ͨ������������ó��˿ɽ���B��C�еķ�Ӧ���⣬���У�_____��
��4��C�з�Ӧ���ɳ��������ӷ���ʽ��________��
��5�����и����ʩ�У�������߲ⶨȷ�ȵ���___�����ţ���
a���ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2����
b���μ�����˹���
c����A-B֮������ʢ��Ũ�����ϴ��װ��
d����B-C֮������ʢ�б���̼��������Һ��ϴ��װ��
��6��ʵ����ȷ��ȡ8.0g��Ʒ���ݣ��������βⶨ�����BaCO3ƽ������Ϊ3.94 g������Ʒ��̼��Ƶ���������Ϊ__________��
��7��������Ϊ���زⶨC�����ɵ�BaCO3������ֻҪ�ⶨװ��C������CO2ǰ��������һ������ȷ��̼��Ƶ�����������ʵ��֤�����˷����ⶨ�Ľ������ƫ�ߣ�ԭ����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��G��һ���������ϵ���Ҫ�ɷ�֮һ����ṹ�к���������Ԫ����G�ĺϳ�·����ͼ�����ֲ���Ͳ��ַ�Ӧ������ȥ����
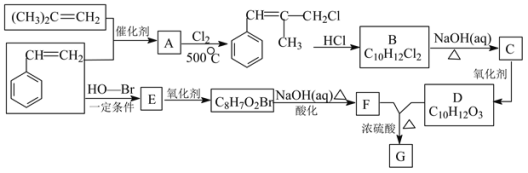
��֪����RCH=CH2+CH2=CHR��![]() CH2=CH2+RCH=CHR��
CH2=CH2+RCH=CHR��
��B�к˴Ź�������ͼ��ʾ��������6�ֲ�ͬ��������ԭ�ӣ�
��D��F��ͬϵ�
��ش��������⣺
(1)(CH3)2C=CH2��ϵͳ����������Ϊ____���÷����������__��ԭ����ͬһƽ���ڡ�
(2)A��B��Ӧ�������漰�ķ�Ӧ��������Ϊ___��___��
(3)D�����к��еĺ���������������___��G�Ľṹ��ʽΪ___��
(4)����E�Ļ�ѧ����ʽΪ____��
(5)ͬʱ������������������FeCl3��Һ������ɫ��Ӧ���ڱ�����������ȡ��������C=O��F��ͬ���칹���ж��֣����к˴Ź�������Ϊ4��塢��ˮ������ʵĽṹ��ʽΪ___��
(6)ģ���ɱ���ϩ�ϳ�F�ķ�����д���ɱ�ϩ��ȡ��-�ǻ����ᣨ![]() ���ĺϳ�·�ߣ�_____��
���ĺϳ�·�ߣ�_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com