
分析 A、B、C、D、E五种短周期的主族元素,它们的原子序数依次递增,A是所有元素中原子半径最小的元素,则A为氢元素,B、C组成的化合物BC2能引起温室效应,则B为碳元素,C为氧元素,常温下,金属D单质投入水中能与水剧烈反应,且D的盐溶液焰色反应显黄色,则D为钠元素,常温下E单质是一种黄绿色气体,则E为氯元素,据此答题.
解答 解:A、B、C、D、E五种短周期的主族元素,它们的原子序数依次递增,A是所有元素中原子半径最小的元素,则A为氢元素,B、C组成的化合物BC2能引起温室效应,则B为碳元素,C为氧元素,常温下,金属D单质投入水中能与水剧烈反应,且D的盐溶液焰色反应显黄色,则D为钠元素,常温下E单质是一种黄绿色气体,则E为氯元素.
(1)根据上面的分析可知,A、B的元素名称分别为氢、碳,故答案为:氢;碳;
(2)E是氯元素,在周期表中第三周期第ⅤⅡA族,故答案为:第三周期第ⅤⅡA族;
(3)同周期自左而右原子半径减小,故原子半径:Na>Cl,故答案为:Na>Cl;
(4)钠在氧气中燃烧生成过氧化钠,反应方程式为:2Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2,故答案为:2Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2;
(5)氯气与水反应的方程式为Cl2+H2O?HCl+HClO,故答案为:Cl2+H2O?HCl+HClO.
点评 本题考查结构性质位置关系应用,关键是推断元素,题目难度不大,侧重对基础知识的巩固.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:解答题
 X、Y、Z三种短周期元素,它们的原子序数之和为16.Z元素的一种原子核内不含中子,X、Y、Z三种元素的常见单质在常温下都是无色、无味气体,在适当条件下可发生如图变化:一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
X、Y、Z三种短周期元素,它们的原子序数之和为16.Z元素的一种原子核内不含中子,X、Y、Z三种元素的常见单质在常温下都是无色、无味气体,在适当条件下可发生如图变化:一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题: ; C分子中所含化学键的类型是极性键,C分子的空间结构呈三角锥形.
; C分子中所含化学键的类型是极性键,C分子的空间结构呈三角锥形.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
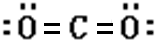 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含磷洗涤剂造成水污染是因为磷的化合物有毒 | |
| B. | 医用酒精消毒是利用了其使蛋白质变性的性质 | |
| C. | 水泥厂、冶金厂应对工厂烟尘进行处理,以减少对空气的污染 | |
| D. | 福尔马林常用于浸制生物标本 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.02 mol | B. | 0.03mol | C. | 0.04mol | D. | 0.06mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
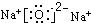
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO3 | B. | NaHSO3 | C. | Na2SO3、NaHSO3 | D. | Na2SO3、NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com