
【题目】医药中间体化合物X的结构简式如图所示。下列有关化合物X的说法正确的是

A.X的分子式为C16H11O4
B.X分子中有三种不同的官能团
C.1 mol化合物X最多能与3 mol NaOH反应
D.X分子中两个苯环一定处于同一平面
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】海洋是一个巨大的资源宝库,海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钠等。可用于制食盐、Mg、Br2、H2、Cl2、NaOH等化工原料。回答下列问题:
(1)Mg元素位于周期表第______周期_______族。
(2)写出NaOH的电子式_______________。
(3)写出电解饱和食盐水的离子方程式:____________。
(4)海水提溴要经过富集、氧化、提取的过程。其中氧化后生成的Br2可用Na2CO3溶液吸收,生成NaBr和NaBrO3及一种气体,写出该反应的化学方程式__________________。
(5)海水提取镁的过程中,得到MgCl2溶液后,先蒸发浓缩、冷却结晶、过滤制得MgCl2·6H2O,然后在HCl气流中加热得到MgCl2,而不是直接蒸发MgCl2溶液的原因是______________。
(6)海洋底部存在的可燃冰,是可开发的中药能源。常温常压下燃烧3.2g甲烷生成液态水,放出178kJ/mol的热量。写出甲烷燃烧的热化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种重要的化工原料,它的产量可以衡量一个国家石油化工水平的高低。A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。

(1)请写出A的结构简式 ;
(2)写出反应B+C→D的化学方程式 ;
(3)使1molA与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生完全取代反应,则两个过程中消耗的氯气的总的物质的量是 mol;
(4)制备D的实验装置图如图所示:收集产物的试管中盛放的液体为 ;
装置中长颈漏斗除起冷凝作用外,另一重要作用是: 。

查看答案和解析>>
科目:高中化学 来源: 题型:
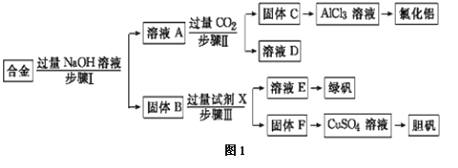
【题目】某工厂的废金属屑的主要成分为铝、铁和铜,某化学兴趣小组在学习了元素及其化合物的相关知识后,设计了如图1实验流程,用该工厂的金属废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O)。
请回答:
(1)写出步骤Ⅱ反应的离子方程式: 。
(2)步骤Ⅰ、Ⅱ、Ⅲ进行的实验操作中均需用到的玻璃仪器有 。
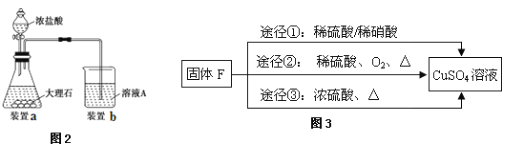
(3)进行步骤Ⅱ时,该小组用如图2所示装置及试剂制取CO2并将制得的气体通入溶液A中一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少,原因是 。
(4)从溶液E得到绿矾晶体的实验操作是 。
(5)用固体F制备CuSO4溶液,可设计如图3三种途径:
写出途径③中反应的化学方程式: ,用途径①制备CuSO4溶液时,混酸中硫酸和硝酸的最佳物质的量之比为 。
(6)用惰性电极电解硫酸铜溶液一段时间后,阴极增重3.2g。请写出阳极电极反应式 ,阳极产生 L气体(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中含有相同的化学键类型的是
A. NaCl、HCl、H2O、NaOH B. Cl2、Na2S、HCl、SO2
C. Na2O2、H2O2、H2O、O3 D. HBr、CO2、H2O、CS2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态Cu2+的核外电子排布式为 ,在高温下CuO 能分解生成Cu2O,试从原子结构角度解释其原因: 。根据元素原子的外围电子排布特征,可将周期表分成五个区域,元素Cu属于 区。
(2)下列叙述不正确的是 。(填字母)
a.HCHO和CO2分子中的中心原子均采用sp杂化
b.因为HCHO与水分子间能形成氢键,所以HCHO易溶于水
c.C6H6分子中含有6个σ键和1个大π键,C2H2是非极性分子
d.CO2晶体的熔点、沸点都比二氧化硅晶体的低,原因是CO2为分子晶体而二氧化硅是原子晶体
(3)氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。其中的C的杂化类型为 ,写出一种与 CN— 互为等电子体的单质分子式 。
(4)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
① 与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 。
② 六氰合亚铁离子[Fe(CN)6]4 -中不存在 。
a.共价键
b.非极性键
c.配位键
d.σ键
e.π键
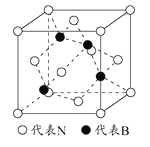
(5)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其晶胞结构与金刚石类似,一个该晶胞中含有 个氮原子, 个硼原子,设氮原子半径为a pm,硼的原子半径b pm ,求该晶胞的空间利用率 。(用含a、b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中的杂质(括号内的物质)除去时,所使用的试剂和主要操作都正确的是( )
选项 | 物质 | 使用的试剂 | 主要操作 |
A | 乙醇(水) | 金属钠 | 过滤 |
B | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
C | 苯(苯酚) | 浓溴水 | 振荡、分液 |
D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com