
 的立体构型为 。
的立体构型为 。 
 a
a 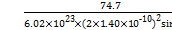 =1.83×10-3
=1.83×10-3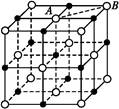
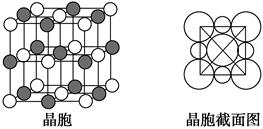
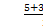 =0,为sp3杂化,正四面体;(6)如图两个最近的阳离子核间的距离为AB;作辅助线,BD垂直AD,∠DAB="60°,BD=AB" sin 60°,设横向上有x个氧离子,纵向上有y个氧离子,横、纵向的长分别为2x·1.40×10-10m、2y·1.40×10-10 m,2x·1.40×10-10 m×2y·1.40×10-10 m×sin60°="1" m2,所以每平方米面积上
=0,为sp3杂化,正四面体;(6)如图两个最近的阳离子核间的距离为AB;作辅助线,BD垂直AD,∠DAB="60°,BD=AB" sin 60°,设横向上有x个氧离子,纵向上有y个氧离子,横、纵向的长分别为2x·1.40×10-10m、2y·1.40×10-10 m,2x·1.40×10-10 m×2y·1.40×10-10 m×sin60°="1" m2,所以每平方米面积上
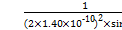 个,NiO的物质的量为
个,NiO的物质的量为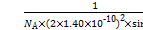 mol,即可求出质量
mol,即可求出质量

 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 =1.732)
=1.732)
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com