
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如图所示变化规律(p表示压强,T表示温度,n表示物质的量): 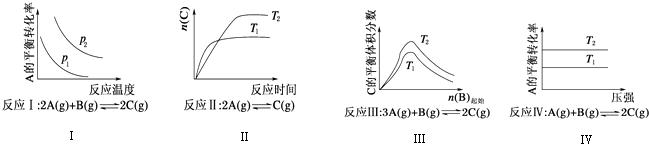
根据以上规律判断,下列结论正确的是( )
A.反应Ⅰ:△H>0,p2>p1
B.反应Ⅲ:△H>0,T2>T1或△H<0,T2<T1
C.反应Ⅱ:△H>0,T1>T2
D.反应Ⅳ:△H<0,T2>T1
【答案】B
【解析】解:A.反应Ⅰ的特点是正反应方向为气体体积减小的方向,结合图象,压强增大A的转化率应增大,所以p2>p1 , 它随温度的升高A的转化率降低,所以正反应为放热反应△H<0,故A错误.B.关于反应Ⅲ,由图象可以看出,T2条件下C的平衡体积分数大,因此当T2>T1时正反应为吸热反应△H>0,而当T2<T1时正反应为放热反应△H<0,故B正确;
C.关于反应Ⅱ由图象可以看出T1条件下达到平衡所用的时间少,所以T1>T2 , 而在T1条件下达平衡时n(C)小,所以说明低温有利于C的生成,故它主要的正反应为放热反应△H<0,故C错误;
D.关于反应Ⅳ,由图象可以看出T2条件下A的转化率大,因此当T2>T1时,说明升高温度平衡向正反应方向进行,因此正反应为吸热反应△H>0,故D错误.
故选B.
【考点精析】根据题目的已知条件,利用化学平衡状态本质及特征的相关知识可以得到问题的答案,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
【题目】Fe 和 Fe2O3 的混合物共 27.2g,加入 200mL 稀 H2SO4,在标准状况下收集到 2.24LH2,Fe和 Fe2O3 均无剩余。为中和过量的 H2SO4,并使 Fe 元素全部转化为 Fe(OH)2 沉淀,消耗了 400mL 3mol/L 的 NaOH 溶液,则该 H2SO4 的物质的量浓度为
A. 3mol/L B. 2.25mol/L C. 2mol/L D. 0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝.电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用.
请回答:
(1)已知:2Al2O3(s)═4Al(g)+3O2(g)△H1=3351KJmol﹣1
2C(s)+O2(g)═2CO(g)△H2=﹣221KJmol﹣1
2Al(g)+N2(g)═2AlN(s)△H3=﹣318KJmol﹣1
碳热还原Al2O3合成AlN的总热化学方程式是___________________________。
(2)在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1:4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比).
反应ⅠCO2(g)+4H2(g)![]() CH4(g)+2H2O(g)△H4
CH4(g)+2H2O(g)△H4
反应ⅡCO2(g)+H2(g)![]() CO(g)+H2O(g)△H5
CO(g)+H2O(g)△H5
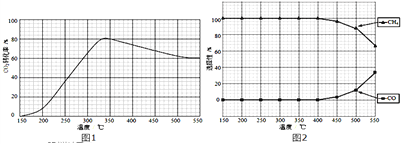
①下列说法不正确的是_______
A.△H4小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1:3,可提高CO2平衡转化率
②350℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为VL该温度下反应Ⅰ的平衡常数为______(用a、V表示)
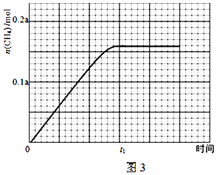
③350℃下CH4物质的量随时间的变化曲线如图3所示.画出400℃下0~t1时刻CH4物质的量随时间的变化曲线_______.
(3)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中氯离子的物质的量浓度与50 mL1 mol·L-1AlCl3溶液中氯离子的物质的量浓度相等的是
A. 150 mL 3 mol·L-1氯酸钠溶液 B. 75 mL 3 mol·L-1氯化钙溶液
C. 150 mL 3 mol·L-1氯化钾溶液 D. 50 mL 3 mol·L-1氯化镁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一学习小组用100g某硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)制备绿矾(FeSO47H2O),主要流程如图: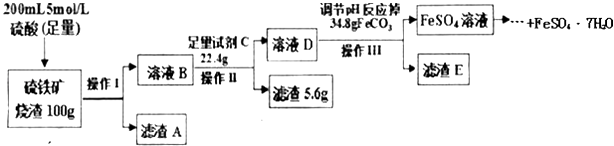
请回答下列问题:
(1)硫铁矿烧渣中加入硫酸酸浸往往需要升温,目的是 , 操作1的名称是 , 滤渣A是 .
(2)试剂C为 , 加入该试剂的目的是(用离子方程式表示).
(3)调节溶液D的pH目的是 .
(4)己知常温下Al(OH)3的Ksp=1.0×10﹣33 , 若溶液中c(Al3+)为1.0mol/L,请计算Al3+开始沉淀的pH= .
(5)依据上述流程中的相关数据,求该硫铁矿烧渣中Fe2O3的质量分数为 . (本实验各操作中损失的硫酸盐、硫酸及调pH后溶液呈微酸性残留的硫酸忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列叙述正确的是( )
A.pH等于5的HCl溶液和pH值等于9的NaOH溶液由水电离出的c(H+)之比为1:1
B.两种醋酸溶液的物质的量浓度分别为c1和c2 , pH分别为a和a+1,则c1=10c2
C.pH=2的HNO3溶液和pH=10的Ba(OH)2溶液等体积混合后的溶液的PH=7
D.向0.1mol/L的氨水中加入少量醋酸铵固体,则溶液中 ![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下图所示的装置及药品进行比较酸性强弱的实验,一段时间后试管②中有胶冻状物质生成。下列说法正确的是( )
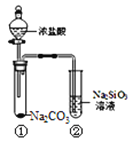
A. 用带有玻璃塞的试剂瓶盛装Na2SiO3溶液
B. 试管①中反应的离子方程式是:Na2CO3+ 2H+ = 2Na+ + CO2↑+ H2O
C. 该实验可以证明酸性:盐酸>碳酸>硅酸
D. 若将盐酸换成硫酸,能证明酸性:硫酸>碳酸>硅酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | Q | R |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(1)Z在元素中期表中的位置是______________________________。
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是__________(填离子符号)。
(3)周期表中有些处于对角线(左上→右下)位置的元素,它们的单质及其化合物的性质相似,则M的氧化物与强碱溶液反应的离子方程式______________________________。
(4)Q和R按原子个数比1:1组成的化合物甲是一种“绿色”氧化剂。
①甲中所含共价键类型是____________________。
②空气阴极法电解制备甲的装置如图所示。在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液。图中a是__________极,阴极的电极反应式是____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中Cl-浓度最小的是 ( )
A. 1000mL 2.5mol/L NaCl溶液 B. 200mL 2mol/L MgCl2溶液
C. 300mL 5mol/L KCl溶液 D. 250mL 1mol/L AlCl3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com