
分析 标况下,气体摩尔体积是22.4L/mol,氮气体积=$\frac{m}{M}{V}_{m}$,每个氮气分子中含有10个电子、3个H原子,根据N=nNA计算氨气分子个数;
根据N=nNA计算水分子个数,每个水分子中含有10个电子;
标况下67.2LHCl的物质的量=$\frac{V}{{V}_{m}}$,据N=nNA计算HCl分子个数,根据m=nM计算HCl质量.
解答 解:标况下,气体摩尔体积是22.4L/mol,氮气体积=$\frac{m}{M}{V}_{m}$=$\frac{1.7g}{17g/mol}×22.4L/mol$=2.24L,氨气分子个数N=nNA=$\frac{1.7g}{17g/mol}$×NA/mol=0.1NA;每个氮气分子中含有10个电子、3个H原子,所以电子物质的量为1mol、H原子个数为0.3NA;
水分子个数N=nNA=0.1mol×NA/mol=0.1NA,每个水分子中含有10个电子,所以电子总数为NA;
标况下67.2LHCl的物质的量=$\frac{V}{{V}_{m}}$=$\frac{67.2L}{22.4L/mol}$=3mol,N(HCl)=nNA=3mol×NA/mol=3NA,m(HCl)=nM=3mol×36.5g/mol=109.5g,
故答案为:2.24L;1;0.3NA;0.1NA;3mol;3NA;109.5g.
点评 本题考查物质的量有关计算,为高频考点,明确各个物理量关系及分子构成是解本题关键,易错点是分子构成,题目难度不大.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
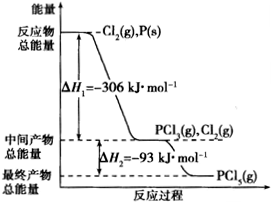 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中△H的表示生成1mol产物的数据).
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中△H的表示生成1mol产物的数据).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol 任何气体的体积都约为22.4L | |
| B. | 1mol 任何物质在标准状况下所占的体积都约是22.4L | |
| C. | 标准状况下,1mol 水所占有的体积是22.4 L | |
| D. | 标准状况下,22.4L的任何气体的物质的量都约是1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
; .
. 是一种重要的药物合成中间体,请结合题目所给信息,
是一种重要的药物合成中间体,请结合题目所给信息, 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 | |
| B. | 除去乙酸乙酯中少量的乙酸:用氢氧化钠溶液洗涤,分液、干燥、蒸馏 | |
| C. | 除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶 | |
| D. | 除去乙烷中少量的乙烯:光照条件下通入Cl2,使乙烯转化成液态二氯乙烷而与乙烷分离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com