
实验室现需物质的量浓度为1 mol·L-1的NaOH溶液480 mL.
(1)要配制此溶液,需要称量的NaOH固体的质量为________.
(2)配制过程中,已有下列仪器:
A.烧杯
B.量筒
C.胶头滴管
D.玻璃棒
E.托盘天平(含砝码)
F.药匙,根据实验的需要,完成实验还缺少的仪器是________
(3)配制过程有如下操作步骤:
①溶解:反称量好的确良NaCl晶体放入小烧杯中,加适量蒸馏水溶解;②移液;③洗涤;④定容;⑤摇匀:将容量瓶塞紧,充分摇匀.
请填写下列空白:
A.要进行第③步操作的目的是:________
B.第④步的具体操作是:________
(4)下列操作会使配制的溶液浓度偏低的是________(填字母)
A.没有将洗涤液转移到容量瓶
B.转移过程中有少量溶液溅出
C.容量瓶洗净后未干燥
D.定容时俯视刻度线
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
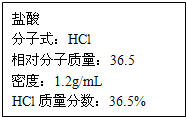 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:| 1000Vd |
| 22400+36.5V |
| 1000Vd |
| 22400+36.5V |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| ||
. |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com