
下列关于元素性质的有关叙述中不正确的是
A. S Cl F H的原子半径依次减小
B. Na Mg Al Si的失电子能力依次增强
C. C N O F的气态氢化物的稳定性依次增强
D. Si P S Cl的最高价氧化物的水化物的酸性依次增强
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+ 对于该平衡,下列叙述正确的是 ( )
CH3COO-+H+ 对于该平衡,下列叙述正确的是 ( )
A.加入少量NaOH固体,平衡向逆反应方向移动
B.升高温度,平衡向正反应方向移动
C.加入水稀释,溶液中c(H+)一定增大
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇:
( CO2 + 3H2 = CH3OH + H2O ),并开发出直接以甲醇为燃料的燃料电池。
已知 H2(g)、 CO(g) 和 CH3OH(l) 的燃烧热△H分别为-285.8 kJ·mol-1、-283.0 kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是_____________kJ
(2)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,实验结果如图所示(注:T1、T2均大于300℃);下列说法正确的是________(填序号)
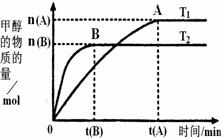 ①温度为T1时,从反应开始到平衡,生成甲醇的
①温度为T1时,从反应开始到平衡,生成甲醇的
平均速率为v(CH3OH)= 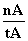 mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时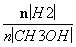 增大
增大
(3)在T1温度时,将1molCO2和3molH2充入一密闭恒容容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为 ( 用 a 表示 )
(4)已知甲醇燃烧的化学方程式为2CH3OH +3O2 =2CO2 +4H2O ,在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为 ,正极的反应式
为
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下在溶液中可发生如下两个离子反应:
Ge4++Fe2+===Fe3++Ge3+, Sn2++2Fe3+===2Fe2++Sn4+
由此可以确定Fe2+、Ge3+、Sn2+三种离子的还原性由强到弱的顺序是 ( )
A.Sn2+、Fe2+、Ge3+ B.Sn2+、Ge3+、Fe2+
C.Ge3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ge3+
查看答案和解析>>
科目:高中化学 来源: 题型:
第29届奥运会祥云火炬的外壳材料是高强度的铝镁合金。某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数,他们利用盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金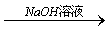 测定生成气体的体积
测定生成气体的体积
方案二:铝镁合金 测定生成气体的体积
测定生成气体的体积
方案三:铝镁合金 溶液
溶液
 称量灼烧产物的质量。
称量灼烧产物的质量。
(1)写出方案一中发生反应的离子方程式 。
(2)实验小组根据方案二设计了两个实验装置,如下圈(图中的铁架台已省略)。
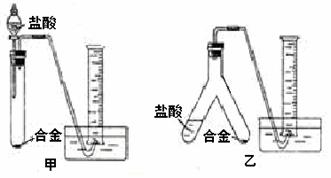
你认为选择 (选填甲或乙)装置进行实验更合理,误差更小。
(3)用方案三进行实验时,除了称量灼烧产物质量外,还需称量的是 。
(4)拓展研究:在向铝镁合金溶于盐酸后的溶液中加入过量NaOH溶液时,生成沉淀的质量与加入NaOH溶液体积的关系可用数轴关系表示:
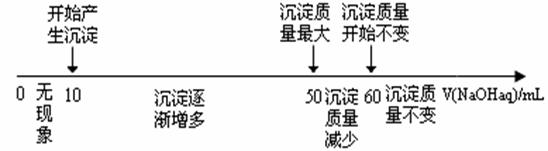
请你判断,根据上图数轴申的数据能否求出合金中镁的质量分数? (选填“能”或“不能”)
下列①②两题选一题作答。
①若不能求出合金中镁的质量分数,请说明理由 。
②若能求出合金中镁的质量分数,则镁的质量分数为 (保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某种气态矿物燃料含有碳、氢两种元素。为了测定这种燃料中碳、氢
两种元素的质量比,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全
部通入下图所示的装置,得到如下表所列的实验结果(假设产生的气体完全被吸
 收)。
收)。
| 实验前 | 实验后 | |
| (干燥剂+U形管)的质量 | 101. 1 g | 102. 9 g |
| (石灰水+广口瓶)的质量 | 312. 0 g | 314. 2 g |
根据实验数据,求:
① 实验完毕后,生成物中水的物质的量为 mol,假设广口瓶里生成一种正盐,其质量为 g;
② 气态矿物燃料中碳元素与氢元素的质量比为 ;
③ 该气态矿物燃料的分子式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某氢氧燃料电池,电极为多孔镍,电解液为30%的KOH溶液,下列有关叙述正确的是
①负极反应为:4OH--4e- =O2↑+2H2O ②负极反应:H2+2OH- - 2e- =2H2O
③工作时正极区pH升高,负极区pH降低 ④工作时溶液中阴离子移向正极
A.③④ B.②③ C.②④ D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com