
科目:高中化学 来源: 题型:
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是( )
A.由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-===AlO2-+2H2O
C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-===Cu2+
D.由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出1 mol Ag时,消耗铜电极32 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式中正确的是 ( )
A.氯气与水反应: Cl2 + H2O= 2H+ +Cl- +ClO-
B.氯气通入氢氧化钠溶液中:2Cl2 + 2OH- =3Cl- +ClO- +H2O
C.氯化亚铁溶液中滴加过量新制氯水:2Fe2+ +Cl2 = 2Fe3+ + 2Cl-
D.少量碳酸钙固体加入足量稀盐酸中:CO32- +2H+ = CO2↑ + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于元素性质的有关叙述中不正确的是
A. S Cl F H的原子半径依次减小
B. Na Mg Al Si的失电子能力依次增强
C. C N O F的气态氢化物的稳定性依次增强
D. Si P S Cl的最高价氧化物的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
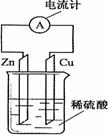
右图为Cu-Zn原电池示意图,下列叙述正确的是
A.锌为负极,发生还原反应
B.铜为负极,铜片上有气泡产生
C.电子由铜片通过导线流向锌片
D.溶液中的H+从铜片获得电子被还原成氢原子
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于100 mL 1 mol/L盐酸与铁片的反应,采取下列措施能使反应速率加快的是:① 升高温度;② 改用100 mL 3 mol/L盐酸;③ 多用300 mL 1 mol/L盐酸;④ 用等量铁粉代替铁片;⑤ 改用98%的硫酸。
A.①②③⑤ B.①②④ C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
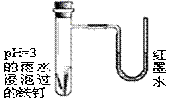
如图是探究铁发生腐蚀的装置图。发现开始时U型管左端红墨水水柱下降,一段时间后U型管左端红墨水水柱又上升。下列说法不正确的是
A.开始时发生的是析氢腐蚀
B.一段时间后发生的是吸氧腐蚀
C.两种腐蚀负极的电极反应均为:Fe-2e—=Fe2+
D.析氢腐蚀的总反应为:2Fe+O2+2H2O=2Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是  ( )
( )
 A.同周期元素中X的金属性最强 B.同周期元素中Y的最高价含氧酸的酸性最强
A.同周期元素中X的金属性最强 B.同周期元素中Y的最高价含氧酸的酸性最强
 C.原子半径X>Y,离子半径X+>Z2- D.同族元素中Z的氢化物稳定性最高
C.原子半径X>Y,离子半径X+>Z2- D.同族元素中Z的氢化物稳定性最高
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(1)用化学用语回答下列问题:
①A元素在周期表中的位置 ;②C单质分子的电子式 ;
③用电子式表示A和B元素组成的化合物的形成过程: 。
(2)元素D与元素A相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为
(其他条件略去)。
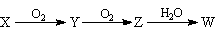
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,生成该白色沉淀的化学方程式为: ;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com