
【题目】下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属, K是一种红棕色气体。
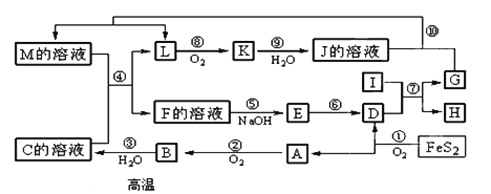
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第____________周期_________族。
(2) 在反应⑦中氧化剂与还原剂的物质的量之比为___________________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是___________(填序号)
(4) 反应④的离子方程式是:__________________________________。
(5) 将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾), 同时还生成KNO2和H2O。该反应的化学方程式是:
_________________________ 。
【答案】(1)四; Ⅷ (2分) (2)1:2(2分) (3)③(2分)
(4)3Fe2+ + NO3- + 4H+= 3Fe3++ NO↑ + 2H2O(2分)
(5)Fe2O3+ 3KNO3+ 4KOH = 2K2FeO4+ 3KNO2+ 2H2O(2分)
【解析】试题分析:FeS2氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,即铝热反应.K是一种红棕色气体,为NO2,则J为HNO3,L被氧化成为NO2,故L可能为氨或NO2,由于C溶液,即硫酸溶液能与某M溶液反应得到L,故L不可能是碱性的气体氨气,故L为NO,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,由反应4FeS2+11O2 ![]() 2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,
2Fe2O3+8SO2,氧化得到的A可以继续被氧化,则A为SO2,B为SO3,C为B的水化物,C为H2SO4,D为Fe2O3,由K是一种红棕色气体,K为NO2,J为HNO3,I为第三主族熔点最高的金属,应为Al,反应⑦为铝单质与金属氧化物所发生的置换反应,G能与硝酸反应并能产生NO,故G为Fe,H为Al2O3,L为NO,M应为Fe(NO3)3或Fe(NO3)2;联系反应④:M+H2SO4 →F+NO↑知,M为Fe(NO3)2,反应中硝酸根有剩余,F为Fe(NO3)3或Fe2(SO4)3,E应为Fe(OH)3,
(1)由以上分析可知G为Fe,是26号元素,位于周期表第四周期第Ⅷ族;
(2)反应⑦为Al与Fe2O3所发生的置换反应,方程式为2Al+Fe2O3![]() 2Fe+Al2O3,氧化铁是氧化剂,铝是还原剂,氧化剂与还原剂的物质的量之比为1:2;
2Fe+Al2O3,氧化铁是氧化剂,铝是还原剂,氧化剂与还原剂的物质的量之比为1:2;
(3)在反应②、③、⑥、⑨中,②、⑥、⑨都为氧化还原反应,③为SO3+H2O=H2SO4的反应,既属于化合反应又属于非氧化还原反应;
(4)M中含有Fe2+和NO3-,在酸性条件下可发生氧化还原反应,反应的离子方程式为3Fe2++4H++NO3-=3Fe3++NO↑+2H2O;
(5)化合物Fe2O3与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O,反应方程式为Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O。


科目:高中化学 来源: 题型:
【题目】金属活动性的强弱与人类开发利用这些金属单质的时间顺序有着某种内在联系。由此推断,下列金属中人类开发利用最早的是:
A.Cu B.Fe C.Zn D.Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验装置如下图所示。先关闭K,使A中的反应进行,加热玻璃管C,可观察到C管中发出耀眼白光,产生白烟,管壁上附着有淡黄色物质。实验完成后,将C管中固体全部加入盐酸中,有臭鸡蛋气味的气体生成。请回答下列有关问题:
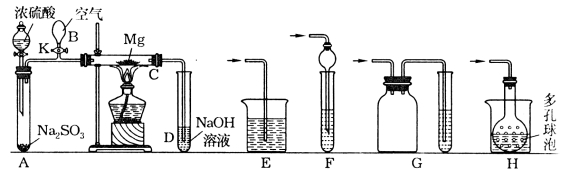
(1)C中全部产物有 、 、 。
(2)本实验先使A中反应进行,再加热C装置,其目的是 。
(3)停止实验时,先打开K,再停止滴加浓硫酸,熄灭酒精灯,橡胶气胆B在实验中的作用是 。
(4)若无装置B、K,使用普通导管,本实验的尾气吸收装置可以选用上图中装置 (填写序号,多选扣分)。
(5)C中的Mg应放在不锈钢垫片上而不能直接接触管壁的原因是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1 mol·L-1 NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是①__________(填序号),配制上述溶液还需用到的玻璃仪器是②____________(填仪器名称)。
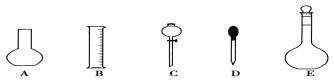
(2)根据计算用托盘天平称取NaOH的质量为③ g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度④__________0.1 mol·L-1(填“大于”、“等于”或“小于”)。
(3)由计算知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为__⑤__mL(计算结果保留一位小数)。如果实验室有15 mL、20 mL、50 mL量筒,应选用__⑥__mL量筒最好。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是将浓硫酸沿烧杯壁缓缓倒入水中,并用玻璃棒不断搅拌。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 Mg、Al、Fe、Cu都是重要的金属元素。下列说法正确的是( )
A.四者对应的氧化物均为碱性氧化物
B.四者的单质放置在空气中均只生成氧化物
C.常温下,Al、Fe不与浓硝酸反应,而Cu能与浓硝酸、稀硝酸反应
D.Fe分别与氯气和稀盐酸反应所得氯化物不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空: ,
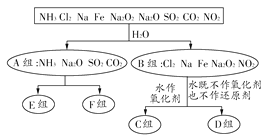
(1)上述第一级分类标准(分成A、B组所依据)是______。
(2)C组物质为______________(填化学式)。
(3)D组物质中,与水反应时氧化剂和还原剂的物质的量之比为1:1的物质是_________(填化学式)。
(4)若E组和F组均有两种物质,则其分类依据是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应速率的说法中,正确的是( )。
A.化学反应速率是指某一时刻、某种反应物的瞬时反应速率
B.化学反应速率为0.8 mol·L-1·s-1指反应1 s时某物质的浓度为0.8 mol·L-1
C.根据化学反应速率的大小可以推知化学反应的快慢
D.对于一个化学反应来说,其反应速率越大,反应现象就越明显
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用地壳中某主要元素生产的多种产品在现代高科技中占有重要位置,足见化学对现代物质文明的重要作用。例如:光导纤维的主要成分是 ;目前应用最多的太阳能电池的光电转化材料是 ;
(2)某气态氧化物的化学式为XO2,在标准状况下,1.92 g 该氧化物的体积为672 mL,则该氧化物的摩尔质量为 _____。
(3)某无色溶液X,由K+、NH4+、Ba2+、Al3+、Fe3+、CO32-、SO42-中的若干种离子组成,取该溶液进行如下实验:
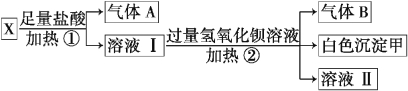
(1)白色沉淀甲是________。
(2)试写出实验过程中生成气体B的离子方程式 _________________________。
(3)通过上述实验,可确定X溶液中一定存在的离子是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com