
【题目】设NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.常温常压下,等物质的量的N2和CO所含分子数均为NA
B.将含0.l mol FeCl3的饱和溶液制成胶体后,生成的Fe(OH)3胶粒数目为0.1NA
C.常温常压下,lmolNa 加热后生成的Na2O、Na2O2混合物中阴离子数目一定为0.5NA
D.1molFe与足量水蒸气在高温下充分反应后失电子数为NA
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.56gN2与CO的混合物中原子总数是4NA
B.0.1mol/L的硫酸溶液中含H+的数目为0.2 NA
C.3mol单质Fe完全燃烧转变为Fe3O4,Fe得到8NA个电子
D.标准状况下,22.4L SO3所含的氧原子数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下。下列说法正确的是( )
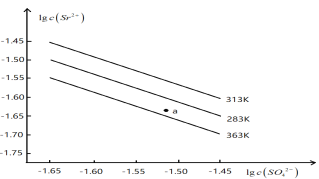
A. 温度一定时, Ksp(SrSO4)随c(SO42-)的增大而减小
B. 三个不同温度中,313 K时Ksp(SrSO4)最大
C. 363 K时,图中a点对应的溶液是不饱和溶液
D. 283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的氧化物(FexO)1.52 g溶于足量盐酸中,向所得溶液中通入标准状况下112 mL Cl2,恰好将Fe2+完全氧化。下列说法正确的是( )
A. FexO溶于足量盐酸后只生成了FeCl3和H2O
B. 标准状况下112 mL Cl2的物质的量是5 mol
C. x=0.8
D. 通入Cl2后,发生反应的离子方程式:Fe2++Cl2![]() Fe3++2Cl﹣
Fe3++2Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要漂白剂,实验室可按下图装置制取NaClO2晶体。

已知:Ⅰ.A中发生的反应为:2ClO2+H2O2+2NaOH=2NaClO2+O2+2H2O
Ⅱ.NaClO2受热易分解,温度高于60℃时分解成NaClO3和NaCl。
(1)已知ClO2与Cl2类似具有漂白性,请设计检验ClO2漂白性的实验方案______。
(2)A中用冰水浴的目的是______。
(3)装置B的作用是______。
(4)测定样品中NaClO2的质量分数的实验过程如下:
步骤一:称0.5000 g样品,加入适量蒸馏水和过量的KI晶体和硫酸,发生如下反应:ClO![]() +4I﹣+4H+=2H2O+2I2+Cl﹣
+4I﹣+4H+=2H2O+2I2+Cl﹣
步骤二:将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液作指示剂,用0.2000 mol·L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为15.00 mL(滴定过程中发生反应:I2+2S2O32-=2I﹣+S4O62-)。
①配制100 mL 0.2000 mol·L-1Na2S2O3标准溶液需要用到的玻璃仪器有烧杯、胶头滴管、______。
②请计算所称取样品中NaClO2的质量分数_______________。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜矾(主要成分 CuSO4·5H2O)是一种可用于食品添加的铜强化剂。现以某硫铁矿渣(含有 CuSO4、CuSO3、Cu2O及少量难溶于酸的Cu2S、CuS)制备铜矾的工艺过程如下:
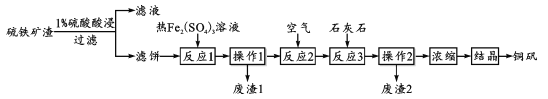
(1)“1%硫酸酸浸”时,固液质量比为1:3并进行4~6次浸取,其目的是_________;
(2)“滤饼”中含有Cu,其中Cu在“反应1”中溶解的离子方程式为________;“废渣1”中只含有S单质,则“反应1”中Cu2S与Fe2(SO4)3反应的物质的量之比为_______。
(3)“反应2”中通入空气的目的是_______;结合离子方程式,说明“反应3”加入石灰石的作用________。
(4)为了提高硫铁矿渣的利用率和产品的产率,在“浓缩”前进行的必要操作是_____;分析下列溶解度信息,最适宜的结晶方式为_________。
t/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 |
CuSO4·5H2O/(g/100g H2O) | 23.1 | 27.5 | 32.0 | 37.8 | 44.6 | 61.8 | 83.8 |
(5)将铜矾、生石灰、水按质量比依次为1.0:0.56:100混合配制无机铜杀菌剂波尔多液,其有效成分为CuSO4·xCu(OH)2·yCa(OH)2。当x=1时,试确定y的值为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,下列说法不正确的是
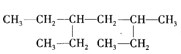
A.该有机物属于饱和链烃
B.该烃的名称是2,4-二乙基己烷
C.该烃与2,5-二甲基-3-乙基己烷互为同分异构体
D.该烃的一氯代物共有8种
查看答案和解析>>
科目:高中化学 来源: 题型:
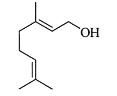
【题目】单萜类化合物香叶醇是香精油的主要成分之一。在酸性溶液中,香叶醇可以转化为环状单萜α—松油醇:
![]()
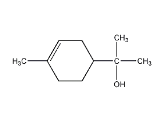
关于香叶醇和α—松油醇,下列说法正确的是( )
A.香叶醇能在铜丝催化下和氧气氧化生成醛,但α—松油醇不能
B.两者互为同分异构体,分子式是C10H20O
C.两者分子中所有原子均处于同一平面
D.两者均能使溴的四氯化碳溶液褪色,是发生消去反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com