
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 电子数 | 10 | 14 | 16 | 18 |
| A、四种气体中至少有两种气体互为同分异构体 |
| B、四种气体通入Br2的CCl4溶液中,都能使其褪色 |
| C、气体丙分子中的所有原子在同一平面 |
| D、鉴别乙和丙两种气体,可以用酸性高锰酸钾溶液 |


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
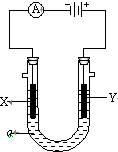 如图表示一个精炼粗铜的电解池,电解液a选用CuSO4溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个精炼粗铜的电解池,电解液a选用CuSO4溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO和N2互为等电子体,常温常压下,22.4L的CO与1monN2所含的电子数相等 |
| B、7.8gNa2S和Na2O2的混合物中含有的阴离子数大于0.1N |
| C、1.0L0.1mol/L的醋酸溶液中含CH3COOH、CH3COO-粒子总数为0.1NA |
| D、5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、绿色化学的核心是应用化学原理对环境污染进行治理 |
| B、春节是我国传统的节日,应把“爆竹声声辞旧岁,总把新桃换旧符”发扬光大 |
| C、近期H7N9型禽流感又在蔓延,应少吃熟的家禽食品 |
| D、“雾霾天气”“温室效应”“光化学烟雾”“PM2.5”等都与汽车尾气排放有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、还原剂 |
| B、氧化剂 |
| C、既是氧化剂又是还原剂 |
| D、既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
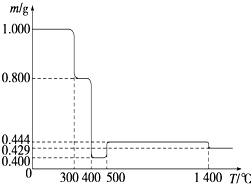 将1.000g FeC2O4?2H2O固体样品放在热重分析仪中进行热重分析,测得其热重分析曲线(样品质量随温度变化的曲线)如图所示:
将1.000g FeC2O4?2H2O固体样品放在热重分析仪中进行热重分析,测得其热重分析曲线(样品质量随温度变化的曲线)如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| A | 原子核外有7种运动状态不同的电子 |
| B | 其一种单质被称为地球生物的“保护伞” |
| C | 常见的金属,在周期表中周期序数与族序数相等 |
| D | 气态氢化物及最高价氧化物对应的水化物均为强酸 |
| E | 一种核素的质量数为56,中子数为30 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com