
����Ŀ��X��Y��WΪԭ���������ε����Ķ�����Ԫ�أ�X��Yͬ���壬Y��W ����̬�⻯�������ͬ�ĵ�������XԪ�ؿ������M��N������̬���ʣ���Ӧ M + 2I-+ 2H+= I2 + N + H2O ����Ϊ M �ļ�����Ӧ��
(1)M��N�Ĺ�ϵΪ_____________________
(2)д��ʵ������ȡW2�����ӷ���ʽ____________________________ ��
(3)�����һij��ѧ��ȤС�������ͼ��ʾ��ʵ��װ��(ͼ�мгֺͼ���װ����ȥ)���ֱ�̽�� YX2��W2 �����ʡ�

�ٷֱ�ͨ�� YX2 �� W2 ʱ����װ�� A �й۲쵽�������Ƿ���ͬ��__________(���ͬ������ͬ��)��
��װ�� D ��װ�������ۣ���ͨ�� W2 ʱ�۲쵽������Ϊ_______________________________________�� ��װ�� D ��װ��������������(V2O5)����ͨ�� YX2 ʱ���� K ������������������ D װ���з�����Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
����װ�� B ��װ�� 5.0 mL 1.0��10-3 mol/L �ĵ�ˮ����ͨ������W2��ȫ��Ӧ��ת����5.0��10-5mol���ӣ��÷�Ӧ�Ļ�ѧ����ʽΪ_______________________________
(4)ijͬѧ�������� YX2 ͨ��һ֧װ�� BaCl2 ��Һ���Թܣ�δ���������ɣ�����Թ��м�������(����ĸ) ___________�����Կ�����ɫ����������
A.��ˮ B.ϡ����C.ϡ���� D.CaCl2 ��Һ
(5)��Y��X��ɵĸ�����������Z��Z��Y��X��������Ϊ Y��X = 4��3���� W2 �뺬Z����Һ��ȫ��Ӧ���л�ɫ�������ɣ�ȡ�ϲ�[Һ���� BaCl2 ��Һ���а�ɫ�����������÷�Ӧ�����ӷ���ʽΪ______________________________________��
���𰸡� ͬ�������� MnO2 + 2Cl- + 4H+![]() Mn2++ Cl2��+ 2H2O ��ͬ �����ػ�ɫ����
Mn2++ Cl2��+ 2H2O ��ͬ �����ػ�ɫ���� ![]() 5Cl2 + I2 + 6H2O = 2HIO3 + 10HCl AC Cl2 + S2O32-+ H2O = S��+ SO42-+ 2Cl- + 2H+
5Cl2 + I2 + 6H2O = 2HIO3 + 10HCl AC Cl2 + S2O32-+ H2O = S��+ SO42-+ 2Cl- + 2H+
��������X��Y��WΪԭ���������ε����Ķ�����Ԫ�أ�X��Yͬ���壬Y��W ����̬�⻯�������ͬ�ĵ���������X��Y��W��Ϊ�ǽ���Ԫ�أ���XΪ�ڶ����ڣ�Y��W�ڵ������ڡ�XԪ�ؿ������M��N������̬���ʣ��ڶ����ڷǽ���Ԫ��ֻ��O���ϣ���Ӧ M + 2I-+2H+=I2+N+H2O����ΪM�ļ�����Ӧ����˵��M�������Ը�ǿ������M��N�ֱ��dz�������������Y��S��Wֻ����Cl��
(1)O3��O2�Ĺ�ϵΪͬ�������壻
(2)ʵ������ȡCl2�����ӷ���ʽΪ��MnO2 + 2Cl- + 4H+ ![]() Mn2++ Cl2��+ 2H2O��
Mn2++ Cl2��+ 2H2O��
(3)��ʵ���Ŀ���Ƿֱ�̽��SO2��Cl2 �����ʡ�
��Aװ����Ҫ��֤�����Ƿ����Ư���ԣ�SO2��Cl2������ʹƷ����ɫ����������ͬ����װ��D��װ�������ۣ���ͨ��Cl2 ʱ�����߿��Է�Ӧ����FeCl3�������ػ�ɫ���̣���װ��D��װ��������������(V2O5)����ͨ��SO2ʱ����K����������������V2O5��������Dװ����SO2��������SO3��������Ӧ�Ļ�ѧ����ʽΪ![]() ��
��
��װ��B��װ��5.0 mL1.0��10-3mol/L�ĵ�ˮ��n��I2��=5��10-6mol��ͨ������Cl2��Cl2��I2��������ȫ��Ӧ��ת����5.0��10-5mol���ӣ�˵��I��0�����ߵ���+5�ۣ�����������HIO3���ʸ÷�Ӧ�Ļ�ѧ����ʽΪ5Cl2+I2+6H2O=2HIO3+10HCl��
(4) ijͬѧ��������SO2ͨ��һ֧װ��BaCl2��Һ���Թܣ�δ���������ɣ�����Թ��м������������������Կ�����ɫ������������ѡAC��
(5)��S��O��ɵĸ�����������Z��Z��Y��X��������Ϊ Y��X = 4��3����Z��S2O32-��
��Cl2�뺬Z����Һ��ȫ��Ӧ���л�ɫ����S���ɣ�ȡ�ϲ�[Һ����BaCl2��Һ���а�ɫ����BaSO4�������ʸ÷�Ӧ�����ӷ���ʽΪ��Cl2+S2O32-+H2O=S��+SO42-+2Cl-+2H+



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. ��������(C3H3N3O3)�ĽṹʽΪ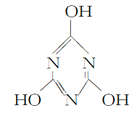 �������ڹ��ۻ�����
�������ڹ��ۻ�����
B. ֻ��H��N��O����Ԫ�صĻ�������������ӻ����Ҳ�����ǹ��ۻ�����
C. NaHCO3��CH3COONa���������Ӽ����ۼ�
D. ������MgO��H2O�л�ѧ����������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(2015���Ϻ����о��绯ѧ��ʴ��������װ������ͼ��ʾ�������й�˵��������ǣ� ��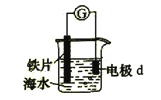
A.dΪʯī����Ƭ��ʴ�ӿ�
B.dΪʯī��ʯī�ϵ缫��ӦΪ��O2 + 2H2O + 4e �� 4OH�C
C.dΪп�飬��Ƭ���ױ���ʴ
D.dΪп�飬��Ƭ�ϵ缫��ӦΪ��2H+ + 2e �� H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���һ�����0.1molL��1�Ĵ�����Һ����μ��˵�Ũ�ȵ�NaOH��Һ����Һ�� pOH[pOH=��lgc��OH����]�� pH �ı仯��ϵ�磬ͼ��ʾ���� �� 
A.M����ʾ��Һ�ĵ�������ǿ��Q��
B.N����ʾ��Һ�� c��CH3COO������c��Na+��
C.Q������NaOH��Һ��������ڴ�����Һ�����
D.M���N����ʾ��Һ��ˮ�ĵ���̶���ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ʵ��С����Ƶ�����ʵ�����������ǣ� ��
A. 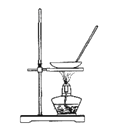 ����NH4Cl������Һ�Ʊ�NH4Cl����
����NH4Cl������Һ�Ʊ�NH4Cl����
B. 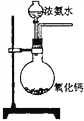 ʵ�����Ʊ���������
ʵ�����Ʊ���������
C. 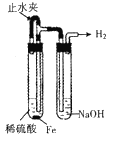 �Ʊ����۲�����������
�Ʊ����۲�����������
D. 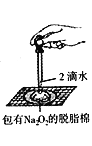 ֤������������ˮ��Ӧ����
֤������������ˮ��Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������10mL 0.1 molL��1NaOH��Һ�м���0.1molL��1��һԪ��HA��ҺpH�ı仯������ͼ��ʾ������˵����ȷ���ǣ� �� 
A.a����ʾ��Һ��c��Na+����c��A������c��H+����c��HA��
B.a��b������ʾ��Һ��ˮ�ĵ���̶���ͬ
C.pH=7ʱ��c��Na+��=c��A����+c��HA��
D.b����ʾ��Һ��c��A������c��HA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���Ʊ����跴Ӧ���Ȼ�ѧ����ʽ���£�SiCl4��g��+2H2��g��Si��g��+4HCl��g������H=+Q kJmol��1��Q��0����ij�¶ȡ�ѹǿ�£���һ������Ӧ��ͨ���ܱ������������Ϸ�Ӧ������������ȷ���ǣ� ��
A.��Ӧ�����У�������ѹǿ�����SiCl4��ת����
B.����Ӧ��ʼʱSiCl4Ϊ1mol�����ƽ��ʱ����������ΪQ kJ
C.��Ӧ��4minʱ����HClŨ��Ϊ0.24 mol/L����H2�ķ�Ӧ����Ϊ0.03 mol/��Lmin��
D.����Ӧ��������Ϊ0.025Q kJʱ�����ɵ�HClͨ��100mL 1molL��1��NaOH��Һǡ�÷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ϊ���ʣ��������õij��ӷ�����ȷ���ǣ�
��������HCl��������ͨ������ʳ��ˮ
��NaCl���壨I2��������
��NaBr��Һ��NaCl������AgNO3��Һ����
����ˮ��I2�����ӱ���ȡ���Һ
A.�٢�B.�ۢ�C.�٢ڢ�D.ȫ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com