
科目:高中化学 来源: 题型:
| 元素代号 | Ⅰ1 | Ⅰ2 | Ⅰ3 | Ⅰ4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 性质或原子结构 |
| A | 原子核内只有一个质子 |
| B | 单质是空气中含量最多的气体 |
| X | 原子的最外层电子数是次外层电子数的3倍 |
| Y | 短周期元素中原子半径最大的元素 |
| Z | 最高正化合价与最低负化合价的代数和为6 |
| ||
| △ |
| ||
| △ |
| 实验操作 | 实验现象 | 结论及解释 |
| ①取少量NaBr 溶液于试管中,滴加 氯水 氯水 ,振荡;②再加入少量CCl4,振荡,静置. |
①溶液由无色变为橙黄色. ②溶液分层, 上层液体几乎为无色,下层液体为橙红色 上层液体几乎为无色,下层液体为橙红色 . |
氧化性:Z 单质>Br2 离子方程式 Cl2+2Br-═2Cl-+Br2 Cl2+2Br-═2Cl-+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | |||||||||||||||||
| D | E | ||||||||||||||||
| G | Q | M | R | ||||||||||||||
| T | |||||||||||||||||
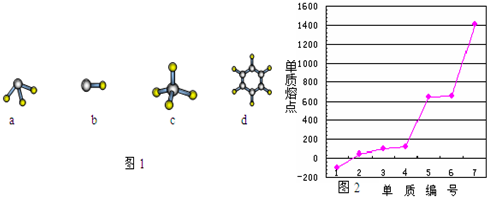
查看答案和解析>>
科目:高中化学 来源: 题型:
 【化学一选修3物质结构与性质】
【化学一选修3物质结构与性质】| 电离能 | I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| (KJ.mol-1) | 14.5 | 29.6 | 47.4 | 77.5 | 97.9 | 551.9 | 666.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
阅读下面一段文字,回答有关问题:
中国科学院近代物理研究所利用重离子加速器提供的丰中子束氧-18轰击天然铀靶,使用奇异的多核子转移反应,在“可裂变核区”合成了重质量丰中子新核素镤-239,这在世界上尚属首次。镤-239是中科院近代物理研究所在质量数大于170的重质量丰中子区合成的第四个新核素。这一成果填补了核素图上又一个空白,为重质量丰中子区的核结构和天文物理研究提供了很有价值的信息。
(1)氧-18原子中质子数是 ,中子数是 ,核外电子数是 ,有 个电子层,最外层有 个电子,最常见化合价为 。
(2)0.2mol氧-18原子的质量是 。
(3)铀元素有 种核素,其中 是制造原子弹的原料。
(4)在“镤-239是中科院近代物理研究所在质量数大于170的重质量丰中子区合成的第四个新核素”这句话中,质量数的含义是 ,核素的含义是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com