
| A. | 原电池负极被氧化 | |
| B. | 任何化学反应都能设计成原电池 | |
| C. | 原电池是一种将化学能转化为电能的装置 | |
| D. | 原电池要使氧化反应和还原反应分别在两个不同的区域进行并形成电流 |
分析 A、原电池的负极发生氧化反应;
B、非氧化还原反应不能设计成原电池;
C、原电池是将化学能转化为电能的装置;
D、原电池负极发生氧化,正极发生还原,外电路电子定向移动形成电流.
解答 解:A、原电池的负极发生氧化反应,被氧化,故A正确;
B、非氧化还原反应不能设计成原电池,并不是所有氧化还原反应都能设计成原电池,故B错误;
C、原电池是将化学能转化为电能的装置,故C正确;
D、原电池负极发生氧化,正极发生还原,外电路电子定向移动形成电流,所以原电池要使氧化反应和还原反应反应分别在两个不同的区域进行并形成电流,故D正确;
故选B.
点评 本题考查了原电池产生电流的本质原因,难度不大,明确原电池是两个极分别发生氧化和还原反应.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:解答题
 早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成.回答下列问题:
早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某中学化学兴趣小组同学为探究元素周期律,设计了如下一系列实验.
某中学化学兴趣小组同学为探究元素周期律,设计了如下一系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸化学式 | CH3 COOH | HCN | H2 CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| B. | Na2CO3和NaHCO3等物质的量混合的溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| C. | 0.4mol/L HCN溶液与0.2mol/L NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-)>c(OH-)>c(H+) | |
| D. | 25℃时,浓度均为0.1mol/L的CH3COONa、CH3COOH混合溶液中:c(Na+)+c(H+)>c(CH3COO-)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+的结构示意图: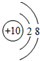 | B. | CO2的球棍模型: | ||
| C. | Na2S的电子式: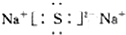 | D. | 乙烯的结构简式:CH2CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ①组 | ②组 |
CH4、聚乙烯、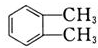 | CH3CH═CHCH3、乙烯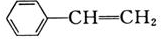 |
| A. | 根据物质是否能使酸性高锰酸钾溶液褪色 | |
| B. | 根据物质是否能发生取代反应 | |
| C. | 根据物质中所有的碳原子是否可以在同一平面内 | |
| D. | 根据物质是否能与溴的四氯化碳溶液发生化学反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com