
【题目】最近科研工作者合成了一种含Si新型阻燃剂F,其合成路线如图:

回答下列问题:
(1)在质谱图中,A的最大质荷比为_____。
(2)B的结构简式为_____,D中所含官能团名称为_____。
(3)C到D的化学反应方程式为_____,反应类型_____。
(4)A有多种同分异构体,其中一种为链状结构,核磁共振氢谱显示有两组峰,且峰面积之比为2:1,其结构简式为_____。
(5)已知:![]() ,根据上述流程,以ClCH2CH=CH2和对甲基苯酚为原料制备
,根据上述流程,以ClCH2CH=CH2和对甲基苯酚为原料制备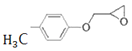 ,写出合成路线_____(无机试剂任选)。
,写出合成路线_____(无机试剂任选)。
【答案】94 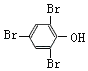 醚键、溴原子
醚键、溴原子 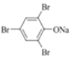 +
+![]() →
→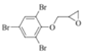 +NaCl 取代反应 HC≡CCH2OCH2C≡CH、H2C=C=CH﹣O﹣CH=C=CH2
+NaCl 取代反应 HC≡CCH2OCH2C≡CH、H2C=C=CH﹣O﹣CH=C=CH2 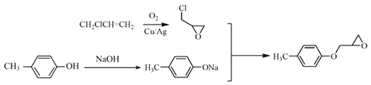
【解析】
由A的分子式、D的结构简式,可知A为![]() ,A与浓溴水发生取代反应生成B为
,A与浓溴水发生取代反应生成B为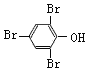 ,B与NaOH发生中和反应生成C为
,B与NaOH发生中和反应生成C为 ,C与
,C与![]() 发生取代反应生成生成D,D与SiCl4发生开环得到E,E与环氧乙烷再发生开环得到F。
发生取代反应生成生成D,D与SiCl4发生开环得到E,E与环氧乙烷再发生开环得到F。
(1)A为![]() ,在质谱图中,A的最大质荷比等于其相对分子质量为94;
,在质谱图中,A的最大质荷比等于其相对分子质量为94;
(2)B的结构简式为 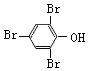 ,D中所含官能团名称为:醚键、溴原子;
,D中所含官能团名称为:醚键、溴原子;
(3)C到D的过程中C中钠原子被取代,化学反应方程式为: +
+![]() →
→ +NaCl,属于取代反应;
+NaCl,属于取代反应;
(4)A(![]() )有多种同分异构体,其中一种为链状结构,核磁共振氢谱显示有两组峰,且峰面积之比为2:1,存在对称结构,A的不饱和度为4,所以可以有2个碳碳三键,结构简式为HC≡CCH2OCH2C≡CH,也可以有4个碳碳双键,结构简式为H2C=C=CH﹣O﹣CH=C=CH2;
)有多种同分异构体,其中一种为链状结构,核磁共振氢谱显示有两组峰,且峰面积之比为2:1,存在对称结构,A的不饱和度为4,所以可以有2个碳碳三键,结构简式为HC≡CCH2OCH2C≡CH,也可以有4个碳碳双键,结构简式为H2C=C=CH﹣O﹣CH=C=CH2;
(5)根据C到D的变化可知由![]() 与
与![]() 反应可得到目标物,而对甲基苯酚与NaOH反应得到
反应可得到目标物,而对甲基苯酚与NaOH反应得到![]() ,ClCH2CH=CH2在催化剂条件下氧化得到
,ClCH2CH=CH2在催化剂条件下氧化得到![]() ,所以合成路线流程图为:
,所以合成路线流程图为: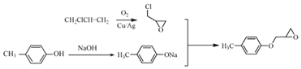 。
。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】芳香族化台物肉桂酸甲酯常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,其球棍模型如图所示(图中球与球之间的棍代表化学键,如单键、双键等)。其制备过程涉及肉桂醇电解制备肉桂醛,肉桂醛氧化制备肉非酸,再与甲醇酯化制得。下列说法不正确的是

A. 肉桂酸甲酯的分子式为C10H10O2
B. 电解肉桂醇制得的肉桂醛在电解池的阴极生成
C. 1mol肉桂酸甲酯与H2加成最多消耗4mol
D. 肉桂酸甲酯中所有碳原子可能在同一平面内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,体积一定的密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度(mol·L-1) | 0.1 | 0.2 | 0 |
平衡浓度(mol·L-1) | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
B.增大压强使平衡向生成Z的方向移动,平衡常数增大
C.反应达到平衡时,X的转化率为50%
D.反应起始时和达平衡时的压强比为3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由U形管、质量为m g的铁棒、质量为m g的碳棒和1 L 0.2 mol·L-1 CuCl2溶液组成的装置如图所示,下列说法正确的是
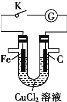
A.打开K,铁棒上有紫红色物质析出
B.闭合K,碳棒上有紫红色固体析出
C.闭合K,当电路中有0.3NA个电子通过时,理论上碳棒与铁棒的质量差为9.6 g
D.闭合K,铁棒表面发生的电极反应为Cu2++2e-=Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合元素周期表,完成下列问题。

(1)在元素周期表中全部是金属元素的区域为____________(填序号)。
a.A b.B c.C d.D
(2)Ⅰ和Ⅱ元素形成的化合物的化学式为__________________,写出其中含有非极性共价键的化合物的电子式_______________。
(3)现有甲、乙两种短周期元素,室温下,甲元素的单质在冷的浓硫酸或空气中表面都会生成致密的氧化膜,乙元素原子核外第三层与第一层上的电子数相等。
①写出甲元素周期表中对应的位置__________。
②甲、乙两元素中,金属性较强的是__________(填元素名称),可以验证该结论的实验是_______________(填序号)。
a.将在空气中放置已久的这两种元素的单质分别放入热水中
b.将这两种元素的单质粉末分别和相同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的容器中进行反应N2(g)+3H2(g) ![]() 2NH3(g),若氮气浓度由0.1 mol·L-1降到0.06 mol·L-1需2 s,那么由0.06 mol·L-1降到0.024 mol·L-1需要的反应时间为
2NH3(g),若氮气浓度由0.1 mol·L-1降到0.06 mol·L-1需2 s,那么由0.06 mol·L-1降到0.024 mol·L-1需要的反应时间为
A. 等于1.8 s B. 等于1.2 s C. 大于1.8 s D. 小于1.8 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。
(1)Cu2+价电子排布式为___________;[Cu(NH3)4]SO4·H2O中,1mol[Cu(NH3)4]2+含有σ键的数目为___________。
(2)SO42-中S原子轨道杂化类型为___________,H3O+几何构型为___________。
(3)NH3极易溶于H2O中,可能的原因为___________。
(4)N、O、S第一电离能由大到小的顺序为___________。

(5)Cu与F形成的化合物的晶胞结构如图所示,若晶体密度为ag·cm-3,则Cu与F最近距离为___________pm(用NA表示阿伏加德罗常数的值,列出计算表达式,不用化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3DZn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3DZn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。
ZnO(s)+2Ni(OH)2(s)。

A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B. 充电时阳极反应为Ni(OH)2(s)+OH(aq)e![]() NiOOH(s)+H2O(l)
NiOOH(s)+H2O(l)
C. 放电时负极反应为Zn(s)+2OH(aq)2e![]() ZnO(s)+H2O(l)
ZnO(s)+H2O(l)
D. 放电过程中OH通过隔膜从负极区移向正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国古代文献中记载了大量古代化学的研究成果,《本草纲目》中记载:“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”,反应原理为:S+2KNO3+3C===K2S+N2↑+3CO2↑。
(1)氮原子的价层电子排布图为___________,烟花燃放过程中,钾元素中的电子跃迁的方式是___________,K、S、N、O四种元素第一电离能由大到小的顺序为___________。上述反应涉及的元素中电负性最大的是___________(填元素符号)。
(2)碳元素除可形成常见的氧化物CO、CO2外,还可形成C2O3(结构式为![]() )。C2O3与水反应可生成草酸(HOOC—COOH)。
)。C2O3与水反应可生成草酸(HOOC—COOH)。
①C2O3中碳原子的杂化轨道类型为___________,CO2分子的立体构型为___________。
②草酸与正丁酸(CH3CH2CH2COOH)的相对分子质量相差2,二者的熔点分别为101℃、-7.9℃,导致这种差异的最主要原因可能是______________________。
③CO分子中π键与σ键个数比为___________。
(3)超氧化钾的晶胞结构图如下:

则与K+等距离且最近的K+个数为___________,若晶胞参数为dpm,则该超氧化物的密度为___________g·cm-3(用含d、NA的代数式表示,设NA表示阿伏加德罗常数的值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com