
����Ŀ��25��ʱ�������й���Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A. 0.1 mol��L��1CH3COONa��Һ��0.1 mol��L��1 HCl��Һ�������ϣ�
c(Na��)=c(Cl��)��c(CH3COO��)��c(OH��)
B. 0.1 mol��L��1 NH4Cl��Һ��0.1 mol��L��1 ��ˮ�������ϣ�pH��7����
c(NH3��H2O)��c(NH4��)��c(Cl��)��c(OH��)
C. 0.1 mol��L��1 Na2CO3��Һ��0.1 mol��L��1 NaHCO3��Һ�������ϣ�
![]() c(Na��) = c(CO32��) + c(HCO3��) + c(H2CO3)
c(Na��) = c(CO32��) + c(HCO3��) + c(H2CO3)
D. 0.1 mol��L��1 Na2C2O4��Һ��0.1 mol��L��1 HCl��Һ�������ϣ�H2C2O4Ϊ��Ԫ���ᣩ��
���𰸡�C
��������
����A������Ϻ�Ϊ�Ȼ��ƺʹ��ᣬ��Һ�д��Ჿ�ֵ���������ӣ�ˮҲ����������ӣ�����������Ũ�ȴ��ڴ��������Ũ�ȣ�����ѡA��B����Ϻ���Һ�Լ��ԣ�˵����ˮ�ĵ������笠����ӵ�ˮ�⣬����Һ笠�����Ũ�ȴ���һˮ�ϰ�Ũ�ȣ�����ѡB��C������̼���ƺ�̼�����Ƶ������غ��������ȷ��ѡC��D�����ߵ������Ϻ�Ӧ���ɵ������Ȼ��ƺͲ������ƣ�������Һ�еĵ���غ��������2c(C2O)��c(HC2O)��c(OH��)��c(Na��)��c(H��)+ c(Cl��)������ѡD��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѹ�£����ķе���ڼױ����۵�ȴ���ڼױ��������۵���ߵ�ԭ�������
A. �����з�����B. ���еĻ�ѧ��ǿ�ȸ�ǿ
C. �����Ӽ���������СD. ��̬ʱ���������и�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A. ʽ����ͬ��������ͬ������
B. ����ʽ��ͬ�IJ�ͬ�л���һ����ͬ���칹��
C. ���һ�����߶����CH2ԭ���ŵ��л�������ͬϵ��
D. �����к���̼����Ļ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��¡����ݵ��ܱ������н��з�ӦA(g)![]() B(g)+C(g)������Ӧ���Ũ����2 mol��L-1����0.8m01��Lһ1��Ҫ20s����ô��Ӧ��Ũ������0��8 mol��L-1����0.2 mol��L-1����Ҫ��ʱ��Ϊ
B(g)+C(g)������Ӧ���Ũ����2 mol��L-1����0.8m01��Lһ1��Ҫ20s����ô��Ӧ��Ũ������0��8 mol��L-1����0.2 mol��L-1����Ҫ��ʱ��Ϊ
A. l0sB. ����10sC. С��10sD. ���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A. ��ˮϡ�ͺ���Һ��![]() ��ֵ��С
��ֵ��С
B. 0.1 mol��L��1Na2CO3��Һ������ˮϡ�ͣ�CO32-��ˮ��̶�������Һ��pH����
C. ��⾫��ͭ�����У����������ļ�������������������һ�����
D. 298 Kʱ��2H2S(g)��SO2(g)=3S(s)��2H2O(l)���Է����У�������H<0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(SO2C12)����������ҽҩƷ��Ⱦ�ϵȡ�ͨ����������۵�Ϊ��54.1�棬�е�69.2�棬��ˮ�������ҷ�Ӧ�����Ȼ������塣ijʵ��С�����ø���������Ͷ��������ڻ���̿������ȡ�����ȣ���ʵ��װ�����£�

(1)�й������ܵ�ʹ��ԭ��������˵����ȷ����(����ĸ)______________��
a�������������ڹܵ������
b��������Һ��ķе㳬��140�棬ˮ����ը����������ʱ����ÿ���������
c�����������ܶ������л��Ʊ��Ļ����������ڷе�ϵ͵�Һ��
d���������Χ���Ŀռ�Ϊ��ˮ�����������������������������ߵĹ���
(2)B�е��Լ�Ϊ___________������Ϊ______________________________��
(3)�ڲ��ı�װ�õ�ǰ���£����е�KClO3����_____________����(�ѧʽ)��
(4)��С����Cu(NO3)2��3H2O�����еμ�SO2C12�Ʊ�������ˮCu(NO3)2��
����д��SO2C12��ˮ��Ӧ�Ļ�ѧ����ʽ__________________________________��
�ڵμ�SO2C12�����ó�����ˮ֮�⣬����_____________________________��
(5)�ⶨ��ˮCu(NO3)2�Ĵ��ȣ����÷ֹ��ȷ����ֲ��[Cu(NH3)4]2+�������A��Cu2+��Ũ�ȹ�ϵ��ͼ��ʾ(��֪4NH3��H2O+Cu2+==[Cu(NH3)4]2++4H2O)��
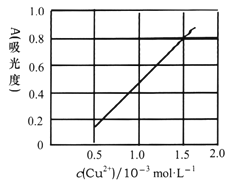
��ȡ0.3150g�Ƶõ���ˮCu(NO3)2��Ʒ��������ˮ�ܽⲢ���Ƴ�100mL��Һ����__________(����������)ȷ��ȡ10��00mL���ӹ�����ˮ����������ˮϡ����100mL������������A=0.8�������ˮCu(NO3)2��Ʒ�Ĵ�����___________(������λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������в����û��Ϸ�Ӧ�ķ����Ƶõ���(����)
��SiO2����H2SiO3����Na2O2����Al(OH)3����FeCl3 ��CaSiO3
A. �٢ۢ� B. �ڢܢ� C. �ڢ� D. �ں͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�������ij�ֻ�ԭ������ʵ�ֵ���
A.H2O2��H2OB.H2��HCl
C.CaCl2��CaCO3D.CO2��CO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����Ƴ�����ĤH2Sȼ�ϵ�أ�ʵ��������H2S������Դ�����������õ�����������ĤH2Sȼ�ϵ�صĽṹʾ��ͼ��ͼ��ʾ������˵������ȷ����
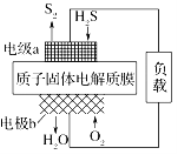
A. �缫aΪ��صĸ���
B. �缫b�Ϸ����ĵ缫��ӦΪO2��4H����4e��===2H2O
C. ��·��ÿ����4 mol���ӣ�����������44.8 L H2S
D. ÿ0.5molH2S���뷴Ӧ����1 mol H��������Ĥ����������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com