
【题目】下列对应的离子方程式正确的是( )
A.酸性高锰酸钾溶液和草酸溶液反应:2![]() +16H++5
+16H++5![]() ═2Mn2++10CO2↑+8H2O
═2Mn2++10CO2↑+8H2O
B.向氯化铁溶液中通入过量二氧化硫:2Fe3++3SO2+6H2O═2Fe+3![]() +12H+
+12H+
C.银和稀硝酸反应:3Ag+4H++![]() ═3Ag++2H2O+NO↑
═3Ag++2H2O+NO↑
D.向氯水中加入碳酸钠:Cl2+![]() ═Cl-+ClO-+CO2↑
═Cl-+ClO-+CO2↑
【答案】C
【解析】
A.草酸是弱酸,酸性高锰酸钾溶液和草酸溶液反应:2![]() +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,故A错误;
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,故A错误;
B.向氯化铁溶液中通入过量二氧化硫生成氯化亚铁:2Fe3++SO2+2H2O═2Fe2++![]() +4H+,故B错误;
+4H+,故B错误;
C.银和稀硝酸反应生成硝酸银、水和NO:3Ag+4H++![]() ═3Ag++2H2O+NO↑,故C正确;
═3Ag++2H2O+NO↑,故C正确;
D.氯气溶于水生成盐酸和次氯酸,盐酸属于强酸,HClO属于弱酸,酸性H2CO3>HClO>![]() ,氯水中加入少量碳酸钠的离子方程式为2Cl2+
,氯水中加入少量碳酸钠的离子方程式为2Cl2+![]() +H2O=CO2↑+2Cl-+2HClO,氯水中加入足量碳酸钠的离子方程式为:Cl2+2
+H2O=CO2↑+2Cl-+2HClO,氯水中加入足量碳酸钠的离子方程式为:Cl2+2![]() +H2O=Cl-+ClO-+2
+H2O=Cl-+ClO-+2![]() ,故D错误;
,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)若电解食盐水时消耗NaCl的质量为234 g,则在理论上最多可得氯气的体积为________升(标准状况)。
(2)若将2 mol的氯气通入足量石灰乳中,理论上可得到次氯酸钙________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |

(1)该反应的离子方程式 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 < (填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50 mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。(一条即可)
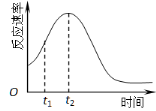 (5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

① ;② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按如图所示要求,完成下列实验:
实验①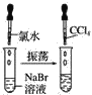
实验②
实验③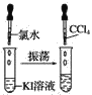
(1)实验①静置后,观察到实验现象是__,反应的化学方程式是__。
(2)实验②静置后,观察到实验现象是__,反应的化学方程式是__。
(3)实验③静置后,观察到实验现象是__,反应的化学方程式是__。
(4)通过上述实验可知,卤素单质氧化性由强到弱的顺序是__,卤素阴离子的还原性由强到弱的顺序是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)铅蓄电池是典型的二次电池,电池总反应式为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________________________。当外电路通过1 mol电子时,理论上负极板的质量增加______g。
2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________________________。当外电路通过1 mol电子时,理论上负极板的质量增加______g。
(二)某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若用HNO3(浓)作电解质溶液,电极为铜片和铝片,正极上发生的电极反应式为________________;
(2)若电解质溶液为0.5mol/LNaOH溶液,电极为镁片和铝片,则负极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M为四种短周期元素。X、Y、Z是原子数依次递增的同周期元素,X与Z可形成常见的XZ或XZ2型分子,Y与M形成的气态化合物对氢气的相对密度为8.5。下列判断正确的是( )
A.最高价含氧酸的酸性:X<Y<ZB.X、Y、Z可形成离子化合物
C.M与Z形成的分子中只有一种共价键D.最简气态氢化物的沸点![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中各组物质不能实现如图所示转化的是
![]()
选项 | 甲 | 乙 | 丙 |
A | CO2 | NaHCO3 | Na2CO3 |
B | AlCl3 | Al2O3 | NaAlO2 |
C | AlCl3 | Al | Al(OH)3 |
D | AlCl3 | Al(OH)3 | NaAlO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X(仅含三种短周期元素)是一种储氢材料,X中某种元素的单质常用来制造信号弹和烟火,某研究小组为了探究X的组成和性质,设计并完成了如下实验。(金属互化物——全部由金属元素组成的化合物)
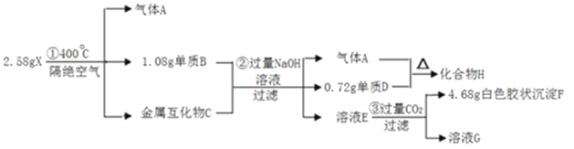
(1)写出H的电子式:________。
(2)X在400℃下分解的化学方程式:________。
(3)下列说法中正确的有:________。
A.化合物H可以与水反应生成氢气 B.单质D可以在干冰中燃烧 C.往溶液E中逐滴加入稀盐酸,将立刻产生白色沉淀 D.溶液G的成分可用于泡沫灭火器
(4)金属化合物C分别与足量盐酸和足量氢氧化钠溶液反应产生的气体物质的量之比为:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇来源丰富,价格低廉,是一种重要的化工原料,有着非常重要、广泛的用途。工业上通常用水煤气在恒容、催化剂和加热的条件下生产甲醇,其热化学方程式为:
2H2(g)+CO(g)![]() CH3OH(g) ΔH=-90.8kJ/mol。
CH3OH(g) ΔH=-90.8kJ/mol。
(1)该反应的平衡常数表达式为:K=______,如升高温度,K值将_____(填:增大、减小或不变)。
(2)以下各项不能说明该反应达到平衡状态的是____________.
A、混合气体的密度保持不变 B、甲醇的质量分数保持不变
C、CO的浓度保持不变 D、2v逆(H2)=v正(CH3OH)
(3)在2100C、2400C和2700C三种不同温度、2L恒容密闭容器中研究合成甲醇的规律。
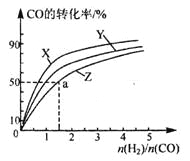
上图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线Z对应的温度是____________。由起始达到a点所需时间为5min,则H2的反应速率____________mol/(L·min)。
(4)某兴趣小组设计了如图所示的甲醇燃料电池装置。

①该电池工作时,正极是_____极(填“a”或 “b”);
②该电池负极反应的离子方程式为____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com