
【题目】硝酸银是一种无色晶体,常用于照相、制镜、印刷、医药等。其水溶液和固体常被保存在棕色试剂瓶中,硝酸银不稳定,受热分解生成固体、NO2和O2。为了研究AgNO3的受热分解产物的性质,某同学设计了以下实验:实验所用的装置如图(图中加热、夹持仪器等均略去):
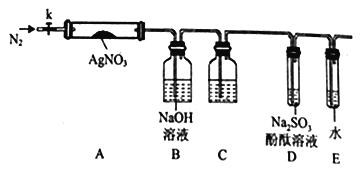
实验步骤为:a.仪器连接后,放入AgNO3固体之前,关闭k,微热硬质玻璃管A。
b.称取AgNO3固体1.7g置于A中,先通入一段时间N2,再关闭k,用酒精灯加热硬质玻璃管A。
c.待样品完全分解,A装置冷却至室温、称量,测得剩余园体的质量为1.08g。……
请回答下列问题:
(1)使用酒精灯对AgNO3固体加热的操作方法是________________________。
(2)步骤a的操作目的是_________________________________________。
(3)步骤b中先通入一段时间N2的操作目的是_______________________________。
(4)装置C瓶中盛装的药品名称为___________,装置D中可观察到的实验现象为___________。
(5)设计实验证明AgNO3分解产物中气体的体积比________________________________。
(6)从实验安全角度考虑该实验装置有缺陷,应如何改进?_____________________。
【答案】 先预热再集中加热 检验装置气密性(检验装置是否漏气) 将容器内部存在的氧气排出,以免影响实验结果 NaOH酚酞溶液 溶液红色变浅(甚至消失) 取足量AgNO3固体充分加热。用排水法收集气体,直到试管内气体不再变化,测量剩余气体占试管容积的比 应在A和B之间加入防倒吸装置(安全瓶)
【解析】(1)先用酒精灯对试管进行均匀受热,然后在集中在有硝酸银的部位加热;正确答案:先预热再集中加热。
(2) 仪器连接后,放入AgNO3固体之前,关闭k,微热硬质玻璃管A,这样操作的目的检验装置是否漏气;正确答案:检验装置气密性或检验装置是否漏气。
(3)容器内部存有空气,用氮气把装置内的空气排净,以免影响实验结果;正确答案:将容器内部存在的氧气排出,以免影响实验结果。
(4)硝酸银受热分解产生的二氧化氮气体被氢氧化钠溶液吸收,是否吸收完全,用C装置进行检验,所以装置C瓶中盛装的药品为NaOH酚酞溶液;装有亚硫酸钠酚酞溶液显红色,氧气与亚硫酸钠反应后变为硫酸钠,溶液呈中性,碱性减弱红色变浅或褪去;正确答案:NaOH酚酞溶液;溶液红色变浅(甚至消失)。
(5)硝酸银受热分解为二氧化氮和氧气,两种气体通入水中发生反应:4NO2+O2+H20=4HNO3,若氧气过量,二氧化氮完全反应;若氧气完全反应,二氧化氮剩余,但最终为一氧化氮气体,根据以上分析可知取足量AgNO3固体充分加热产生的气体用排水法收集,直到试管内气体不再变化,测量剩余气体占试管容积的比,就可以求出AgNO3分解产物中气体的体积比;正确答案:取足量AgNO3固体充分加热。用排水法收集气体,直到试管内气体不再变化,测量剩余气体占试管容积的比。
(6)硝酸银分解产生的二氧化氮气体的量较氧气多,因此,当二氧化氮气体进入装置B中,二氧化氮气体被迅速吸收,容器内压强减小,易产生倒吸,发生危险,因此需要在A和B之间加入防倒吸装置(安全瓶);正确答案:应在A和B之间加入防倒吸装置(安全瓶)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有下列各组微粒或物质:
A、O2和O3
B、 ![]() 和
和 ![]()
C、CH3CH2CH2CH3和 ![]()
D、 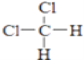 和
和 
E、CH3CH2CH2CH3和 ![]()
(1)________组两种微粒互为同位素;
(2)________组两种物质互为同素异形体;
(3)________组两种物质属于烃;
(4)________组两物质互为同分异构体;
(5)________组两物质是同一物质.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列几个实验,可快速制取实验室所需的少量气体,并进行相关性质实验。(实验装置如图所示)

(1)若B中是生石灰,C中盛有AlCl3溶液,将A中液体逐滴加入B内,实验中观察到C溶液中出现白色沉淀。则A中液体的是_______(填名称),C中发生反应的离子方程式为_________________________。
(2)若要制O2,B为黑色固体,A中的试剂是_________(填化学式),C中盛有FeCl2和KSCN的混合液,旋开分液漏斗的开关后,发现C中溶液变为血红色,同时生成红褐色沉淀。写出C中发生氧化还原反应的离子方程式_______。
(3)已知氧化性强弱:KMnO4>Cl2>KIO3>I2。若A中装有浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,C中的现象是_____________,继续反应一段时间后,发现C中溶液的颜色褪去,这是因为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00 mL,大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
实验编号 | 温度(℃) | 大理石规格 | HNO3浓度(mol/L) | 实验目的 |
① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响;(Ⅱ)实验①和③探究温度对反应速率的影响;(Ⅲ)实验①和④探究________对反应速率的影响 |
② | 25 | 粗颗粒 | _______ | |
③ | _______ | 粗颗粒 | 2.00 | |
④ | _________ | 细颗粒 | ______ |
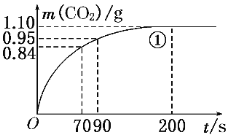
(2)实验①中CO2质量随时间变化的关系见下图。计算实验①中70 s~90 s范围内用HNO3表示的平均反应速率________(忽略溶液体积变化,不需要写出计算过程)。在O~70、70~90、90~200各相同的时间段里,反应速率最大的时间段是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学假说是科学发展的一种重要形式。有科学家提出: 利用空气中的二氧化碳与氢气反应后,使之变为可再生的燃料甲醇的设想。其设想的生产流程如图。下列说法正确的是

A. 上述流程中饱和碳酸钾溶液所起的作用是降低空气中的CO2 的溶解度
B. 上述流程中能体现“循环利用”的物质有碳酸氢钾溶液和高温水蒸气
C. 从合成塔中分离出甲醇的实验操作方法是分液
D. 通入高温水蒸气的作用是: 加快CO2的生成和逸出,以便及时提供给合成塔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用蒸馏水逐步稀释0.2 mol/L的稀氨水时,若温度不变,在稀释过程下列数据始终保持增大趋势的是( )
A.c(OH-) B.c(NH4+) C.c(NH3·H2O) D.c(NH4+)/c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学分析法测得某有机物的化学成分及含量如下表所示,则该物质最可能是()
元素 | C | O | N | H | S | Fe |
含量(%) | 92.393 | 3.518 | 2.754 | 1.214 | 0.006 | 0.006 |
A. 核酸 B. 脂肪 C. 蛋白质 D. 糖类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由2-氯丙烷制取少量1,2-丙二醇时,需要经过下列哪几步反应( )
A.加成→消去→取代B.消去→加成→消去
C.消去→加成→取代D.取代→消去→加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于加成反应的是( )
A. CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
B. CH2===CH2+HCl―→CH3CH2Cl
C. CH3CH2OH+HBr![]() CH3CH2Br+H2O
CH3CH2Br+H2O
D. 2CH3CH3+7O2![]() 4CO2+6H2O
4CO2+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com