
【题目】填写下列空白:
(1)标准状况下,1.1 g某气态氧化物RO2的体积为0.56 L。该气体的摩尔质量是 。
(2)标准状况下,密度为1.25 g·L-1的CO2与CH4组成的混合气体中,CO2的体积分数为 ,该混合气体对氢气的相对密度为 。
(3)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将a g该化合物加热至结晶水全部失去,剩余的残渣为b g,则n= 。
(4)将标准状况下体积为a L的HCl气体溶于1000g水中,得到盐酸的密度为b g/cm3,则该盐酸的物质的量浓度为 mol/L。
【答案】(1)44 g·mol-1 (2)![]() 或42.86% 14
或42.86% 14
(3)![]() (4)
(4)![]()
【解析】
试题分析:(1)根据题意,先由![]() 计算气体的n为
计算气体的n为![]() mol或0.025 mol,再由
mol或0.025 mol,再由![]() 计算该氧化物的M为
计算该氧化物的M为![]() g/mol = 4 4 g/mol;(2)先由M =
g/mol = 4 4 g/mol;(2)先由M = 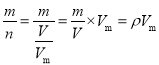 可知,混合气体的平均摩尔质量为1.25×22.4g/mol=28g/mol;再设混合气体中CO2、CH4的物质的量分数或体积分数为x、1-x,则1mol混合气体的质量即等于28g,也等于44x+16(1-x) g,则44x+16(1-x) = 28,解得:x=
可知,混合气体的平均摩尔质量为1.25×22.4g/mol=28g/mol;再设混合气体中CO2、CH4的物质的量分数或体积分数为x、1-x,则1mol混合气体的质量即等于28g,也等于44x+16(1-x) g,则44x+16(1-x) = 28,解得:x=![]() 或42.86%;由
或42.86%;由![]() 可知,同温同压下,该混合气体对氢气的相对密度 =
可知,同温同压下,该混合气体对氢气的相对密度 = ![]() = 14;(3)先由题意和
= 14;(3)先由题意和![]() 可知,A、H2O的物质的量分别为
可知,A、H2O的物质的量分别为![]() mol、
mol、![]() mol,再由化学方程式A·nH2O
mol,再由化学方程式A·nH2O ![]() A + nH2O中水和A的系数之比等于物质的量之比可知,n =
A + nH2O中水和A的系数之比等于物质的量之比可知,n =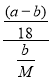 =
=![]() ;(4)先由
;(4)先由![]() 可知,溶质的物质的量为
可知,溶质的物质的量为![]() mol,再由nM可知,溶质的质量为
mol,再由nM可知,溶质的质量为![]() g,然后由m(溶质)+m(溶剂)=m(溶液)、
g,然后由m(溶质)+m(溶剂)=m(溶液)、![]() =V(溶液)可知,V(溶液) =
=V(溶液)可知,V(溶液) = 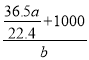 mL =
mL = 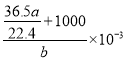 L;最后由
L;最后由![]() 可知,溶质的物质的量浓度为
可知,溶质的物质的量浓度为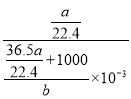 mol/L =
mol/L =![]() mol/L。。
mol/L。。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】某化合物含C、H、O、N等元素,下列哪项最不可能是它的功能 ( )
A. 构成羽毛、肌肉、头发、蛛丝等的成分 B. 催化作用
C. 是细胞内主要的储能物质 D. 构成细胞膜的成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)下列关于实验的叙述中正确的有 (填字母)。
A.不慎碰翻燃着的酒精灯使酒精在桌面上燃烧起来,应立即用湿抹布灭火 |
B.不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗 |
C.先在天平两个托盘上各放一张相同质量的纸,再把氢氧化钠固体放在纸上称 |
D.把试剂瓶中的Na2CO3溶液倒入试管中,发现取量过多,为了不浪费,又把多余的试剂倒入原试剂瓶中 |
E.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
F.使用分液漏斗前要检查其是否漏水
G.用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液中的水全部加热蒸干
(2)某学校实验室从化学试剂商店买回18.4 mol·L-1的硫酸。
现将该浓硫酸配制成100 mL 1 mol·L-1的稀硫酸。可供选用的仪器有:
a.胶头滴管 b.烧瓶 c.烧杯 d.药匙 e.量筒 f.托盘天平
请回答下列问题:
① 配制稀硫酸时,上述仪器中不需要使用的有 (选填序号),还缺少的仪器有 (写仪器名称)。
② 配制100 mL 1 mol·L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为 mL(保留一位小数),量取浓硫酸时应选用 (填序号)规格的量筒。
a.10 mL b.50 mL c.100 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,可以说明恒容密闭容器中的反应:P(g)+Q(g)![]() R(g)+S(g)在恒温下已达平衡状态的是
R(g)+S(g)在恒温下已达平衡状态的是
A.反应容器内压强不随时间变化
B.P和S的生成速率相等
C.反应容器内P、Q、R、S四者物质的量浓度为1:1:1:1
D.反应容器内总物质的量不随时间而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关细胞中元素和化合物的叙述,正确的是 ( )
A. C是构成细胞的基本元素,在人体活细胞中含量最多
B. 脂肪分子中含H比糖类多,是主要的能源物质
C. 氨基酸脱水缩合产生水,水中的氧来自氨基酸的羧基
D. RNA和DNA主要组成元素的种类不同,碱基种类不完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下:

回答下列问题:
(1)钛铁矿和浓硫酸反应的产物之一是TiOSO4,反应中无气体生成。副产品甲阳离子是________。
(2)上述生产流程中加入铁屑的目的是____________________________。
(3)此时溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol·L-1,当溶液的pH等于________时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,写出该反应的离子方程式:________________________。
(4)Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是__________________。(5)在800~1000℃时电解TiO2也可制得海绵钛,装置如图所示。下图中b是电源的________极,阴极的电极反应式________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活息息相关,下列叙述错误的是 ( )
A.铁表面镀锌可增强其抗腐蚀性
B.用聚乙烯塑料代替聚乳酸塑料可减少白色污染
C.大量燃烧化石燃料是造成雾霾天气的一种重要因素
D.含重金属离子的电镀废液不能随意排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切有关,下列说法不正确的是( )
A.Fe2O3常用作红色油漆和涂料
B.氟氯烃是安全、环保的制冷剂
C.聚丙烯酸钠可做“尿不湿”原料
D.硅胶可用作瓶装药品干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
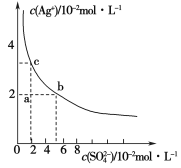
A.a点表示Ag2SO4的不饱和溶液,加入Na2SO4固体不能使溶液由a点变到b点
B.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到c点
C.0.04 mol·L-1的AgNO3溶液与0.2 mol·L-1的Na2SO4溶液等体积混合有Ag2SO4沉淀生成
D.Ag2SO4的溶度积常数(Ksp)为1×10-3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com