
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列属于未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能.
A.①②③④
B.⑤⑥⑦⑧
C.①③⑤⑥⑦⑧
D.③④⑤⑥⑦⑧
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中物质的量浓度为1 mol·L-1的是( )
A.将40 g NaOH固体溶解于1 L水中
B.将22.4 L氯化氢气体溶于水,配成1 L溶液
C.将1 L 10 mol·L-1的浓盐酸与9 L水混合
D.10 g NaOH固体溶解在水中,配制成250 mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取100mL 18.3molL﹣1 的H2SO4与Zn反应,当Zn完全溶解时,生成的气体(可使品红褪色)在标准状况下的体积为22.4L.将所得的溶液稀释成1L,测得溶液H+的浓度为1molL﹣1,则所生成的气体中SO2与H2的体积比约为( )
A.1:2 B.2:1 C.1:4 D.4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的NaHCO3和Na2CO3的混合物放在密闭的容器中加热,充分反应后,测得容器中CO2的体积为4.48L(标准状况)。将反应后的固体与200ml某浓度的盐酸恰好完全反应,转化为8.96LCO2。试回答:(注2NaHCO3![]() Na2CO3 +CO2
Na2CO3 +CO2![]() +H2O)
+H2O)
(1)盐酸的物质的量浓度为多少?__________
(2)原混合物中NaHCO3质量为________;Na2CO3的质量为_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方法错误的是
括号内为杂质 | 实验操作或方法 | |
A. | NO2(NO) | 通入O2 |
B | CuSO4溶液[Fe2(SO4)3] | 加入足量CuO,过滤 |
C | 溴苯(溴) | 加入NaOH溶液,分液 |
D | MnO2(I2) | 加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg—AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl一由正极向负极迁移
D.负极会发生副反应 Mg+2H2O=Mg(OH)2+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在周期表中的相对位置如图所示,已知它们的最外层电子数之和为21,下列说法错误的是( )
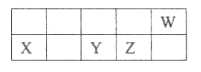
A. 原子半径由大到小的顺序:X、Y、Z、W
B. 元素最高正价由低到高的顺序:X、Y、Z、W
C. 简单氢化物的热稳定性由弱到强的顺序:Y、Z、W
D. 最高价氧化物的水化物的酸性由弱到强的顺序:X、Y、Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2 mol A与2 mol B混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g) ![]() 2C(g)+zD(g);若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g);若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A.v(C)=v(D)=0.2 mol·L-1·s-1
B.z=3
C.B的转化率为75%
D.反应前与2 s后容器的压强比为4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:
(1)配平该反应的离子方程式,并在![]() 中填上所需的微粒。
中填上所需的微粒。
H++ MnO4- + H2C2O4= CO2↑+ Mn2++ ![]()
(2)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为 mol。
(3)测定血钙的含量的方法:取2 mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是 ____________________。
②溶解沉淀时 (“能”或“不能”)用稀盐酸,原因是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com