
| A. | H2O | B. | CH3OH | C. | CS2 | D. | CH3COOH |
科目:高中化学 来源: 题型:选择题
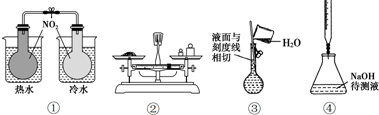
| A. | ①验证温度对平衡移动的影响 | B. | ②称量5.120gNaCl固体 | ||
| C. | ③配制一定物质的量浓度NaCl溶液 | D. | ④中和滴定 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
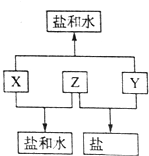 已知:A、B、C、D四种短周期元素,A与D原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,已知Z是常见的两性氢氧化物,试推断回答下列问题.
已知:A、B、C、D四种短周期元素,A与D原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,已知Z是常见的两性氢氧化物,试推断回答下列问题.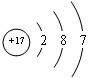 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2(aq)$\stackrel{Cl_{2}}{→}$FeCl3(aq)$\stackrel{Cu}{→}$FeCl2(aq) | B. | H2SO3$\stackrel{△}{→}$Si02$\stackrel{HCl}{→}$SiCl4 | ||
| C. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHC03(s)$\stackrel{△}{→}$Na2CO3(s) | D. | CuS04 $\stackrel{NaOH(aq)}{→}$Cu(OH)2$→_{△}^{乙醛}$Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
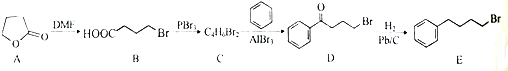
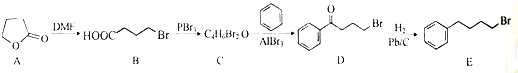
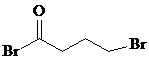 ;由C→D的反应类型是取代反应.
;由C→D的反应类型是取代反应.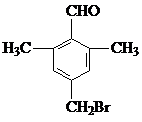 等.
等.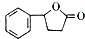 的合成路线流程图(无机试剂任用).合成路线流程图示例如下
的合成路线流程图(无机试剂任用).合成路线流程图示例如下查看答案和解析>>
科目:高中化学 来源: 题型:填空题
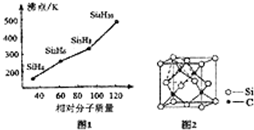
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
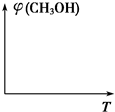 工业上在合成塔中采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=Q kJ•mol-1
工业上在合成塔中采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=Q kJ•mol-1| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
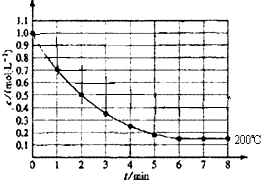 在一密闭容器中放入1molX(g)发生反应:X(g)?4Y(g)+Z(g),如图表示在 200℃时,X的浓度随时间变化的曲线.
在一密闭容器中放入1molX(g)发生反应:X(g)?4Y(g)+Z(g),如图表示在 200℃时,X的浓度随时间变化的曲线.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com