
下列说法正确的是
| A.高熔点的固体如果不是离子晶体,则一定为原子晶体 |
| B.由盐酸的酸性强于氢硫酸的酸性,可推知氧化性:Cl2>S |
| C.由两种元素组成的共价化合物分子中,只可能存在极性键 |
| D.若X+ 和Y2-的核外电子层结构相同,则原子序数:X>Y |
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:单选题
下列说法中正确的是 ( )
| A.CO2、NH3、CCl4、N2 中,所有原子都满足最外层8电子的稳定结构 |
| B.在元素周期表中金属和非金属交界处可以找到半导体材料 |
| C.共价化合物可能含离子键 |
| D.第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、Q、W均为短周期元素,原子序数逐渐增大。X、Q同主族,Q元素的焰色反应为黄色;W的原子半径是同周期中最小的;X与Y、 Z分别形成化合物甲、乙,甲、乙均由10电子分子构成,且能发生反应生成碱。下列说法不正确的是
| A.X的单质和Q的单质均可用电解法得到 |
| B.X与Z可形成同时含有极性键和非极性键的化合物 |
| C.Q与W形成的化合物熔化或溶于水时均可发生电离 |
| D.X、Y、Z三种元素形成的化合物一定能抑制水的电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于原子或离子结构的下列说法不正确的是
| A.某原子K层上只有一个电子 |
| B.某原子M层上电子数为L层上电子数的4倍 |
| C.某离子M层上和L层上的电子数均为K层的4倍 |
| D.某离子核电荷数与最外层电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
13C-NMR (核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构下面叙述正确的是( )
| A.13C与15N有相同的中子数 |
| B.13C与C60互为同位素 |
| C.15N与14N是N元素的两种同位素 |
| D.15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是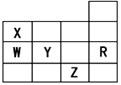
| A.常压下五种元素的单质中Z单质的沸点最高 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物的沸点比X的氢化物的沸点高 |
| D.Y元素的非金属性比W元素的非金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
六种短周期元素A、B、C、D、E、F的原子序数依次增大, C和F同族,B、C、D、E的离子均具有相同的电子层结构,E在同周期元素中离子半径最小。A和B、C、F均能形成共价型化合物,A和B形成的化合物Y在水中呈碱性,D和F形成的化合物在水中呈中性。下列说法错误的是
A.B、D离子的半径大小是B>D
B.C的单质能将F的单质从EF3的溶液中置换出来
C.化合物AC的沸点比化合物AF的高
D.化合物AF与化合物Y可形成含有共价键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是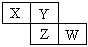
| A.X的气态氢化物比Y的稳定 |
| B.W的最高价氧化物对应水化物的酸性比Z的强 |
| C.Z的非金属性比Y的强 |
| D.X与Y形成的化合物都易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氯元素在自然界有35Cl和37Cl两种同位素,在计算式:34.969×75.77%+36.966×24.23% =35.453中
| A.75.77%表示35Cl的质量分数 |
| B.24.23%表示35Cl的丰度 |
| C.35. 453表示氯元素的相对原子质量 |
| D.36.966表示37Cl的质量数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com