
【题目】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:

下列说法正确的是
A.v1<v2,c2<2c1B.K1>K3,p2>2p3
C.v1<v3,α1(SO2)<α3(SO2)D.c2>2c3,α2(SO3)+α3(SO2)<1
【答案】D
【解析】
针对反应2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热),容器2中加入4mol SO3,等效于在相同温度、相同容积下反应物投入量为4mol SO2、2mol O2,为容器1投入量的两倍,则容器2可看作是先由两个容器1达到平衡后再压缩到容器1的体积,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,p2=2p1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO3)<1,容器1和2的温度相同,则K1=K2;
2SO3(g)(正反应放热),容器2中加入4mol SO3,等效于在相同温度、相同容积下反应物投入量为4mol SO2、2mol O2,为容器1投入量的两倍,则容器2可看作是先由两个容器1达到平衡后再压缩到容器1的体积,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,p2=2p1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO3)<1,容器1和2的温度相同,则K1=K2;
容器3的投入量与容器1相同,温度比容器1高,可以看做是容器1达到平衡后升高温度的新平衡,升高温度反应速率加快,则v1<v3,对于该反应,升高温度平衡逆向移动,则c3<c1,p3>p1,a1(SO2)>a3(SO2),K1>K3,据此分析作答。
针对反应2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热),容器2中加入4molSO3,等效于在相同温度、相同容积下反应物投入量为4molSO2、2molO2,为容器1投入量的两倍,则容器2可看作是先由两个容器1达到平衡后再压缩到容器1的体积,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,p2=2p1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO3)<1,容器1和2的温度相同,则K1=K2;
2SO3(g)(正反应放热),容器2中加入4molSO3,等效于在相同温度、相同容积下反应物投入量为4molSO2、2molO2,为容器1投入量的两倍,则容器2可看作是先由两个容器1达到平衡后再压缩到容器1的体积,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,p2=2p1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO3)<1,容器1和2的温度相同,则K1=K2;
容器3的投入量与容器1相同,温度比容器1高,可以看做是容器1达到平衡后升高温度的新平衡,升高温度反应速率加快,则v1<v3,对于该反应,升高温度平衡逆向移动,则c3<c1,p3>p1,a1(SO2)>a3(SO2),K1>K3,
A. 容器2等效于两个容器1达到平衡后再压缩到容器1的体积达到的平衡,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,,A项错误;
B. 该反应为放热反应,升高温度,平衡逆向移动,则K1>K3,根据分析,p2<2p1,p3>p1,则p2<2p3,B项错误;
C. 容器3看做是容器1达到平衡后升高温度的新平衡,升高温度反应速率加快,则v1<v3,对于该反应,升高温度平衡逆向移动,α1(SO2)>α3(SO2),C项错误;
D. 根据分析,c2>2c1,c3<c1,则c2>2c3,根据分析,α1(SO2)+α2(SO3)<1,a1(SO2)>a3(SO2),则α2(SO3)+α3(SO2)<1,D项正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1molL-1KI溶液:Na+、Ba2+、Fe3+、OH-
B.0.1motL-1Fe2(SO4)3溶液:Zn2+、NH![]() 、Br-、SO
、Br-、SO![]()
C.0.1molL1HNO3溶液:Ba2+、K+、ClO-、Cl-
D.0.1molL-1NaAlO2溶液:Mg2+、Na+、SO![]() 、HCO
、HCO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2与CH4可制得合成气:CH4(g)+CO2(g)2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。初始温度均为T K时,在3个容器中按不同方式投入反应物,发生上述反应,相关信息如下表:
容器 | 起始物质的量/mol | CO2平衡转化率(α) | |||||
编号 | 容积/L | 条件 | CH4(g) | CO2(g) | CO(g) | H2(g) | |
Ⅰ | 2 | 恒温恒容 | 2 | 1 | 0 | 0 | 50% |
Ⅱ | 1 | 0.5 | 1 | 0 | 0 | ||
Ⅲ | 1 | 绝热恒容 | 1 | 0.5 | 0 | 0 | - |
下列说法正确的是
A.T K时,反应CH4(g)+CO2(g)2CO(g)+2H2(g)的平衡常数为1/3
B.容器Ⅱ中反应达到平衡时,α(CO2,Ⅱ)=50%
C.容器Ⅲ中反应达到平衡时反应热在123.5—247 kJ·mol-1范围内
D.容器Ⅱ中反应达到平衡时,再投入0.5 mol CH4、0.25 mol CO,反应达到新平衡前,v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸,Ka1 (H2C2O4 ) =5.4×102,Ka2 (H2C2O4 ) =5.4×105,设H2C2O4溶液中c(总)=c(H2C2O4) +c(HC2O4) +c(C2O42)。室温下用NaOH溶液滴定25.00 mL 0.1000 mol·L1H2C2O4溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是
A. 0.1000 mol·L1 H2C2O4溶液:c(H+ ) =0.1000 mol·L1+c(C2O42 )+c(OH)c(H2C2O4 )
B. c(Na+ ) =c(总)的溶液:c(Na+ ) >c(H2C2O4 ) >c(C2O42 ) >c(H+ )
C. pH = 7的溶液:c(Na+ ) =0.1000 mol·L1+ c(C2O42) c(H2C2O4)
D. c(Na+ ) =2c(总)的溶液:c(OH) c(H+) = 2c(H2C2O4) +c(HC2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OH![]() ClO+Cl+H2O是放热反应。
ClO+Cl+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
(2)步骤Ⅱ合成N2H4·H2O的装置如题19图1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。

(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、![]() 、
、![]() 随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。
随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。

①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置探究Cl2和NO2在NaOH溶液中的反应,若通入适当比例的Cl2和NO2,即发生反应Cl2+2NO2+4NaOH=2NaNO3+2NaCl+2H2O。
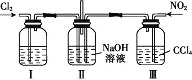
下列叙述正确的是
A. 实验室中用二氧化锰与3 mol·L-1的盐酸共热制备氯气
B. 装置Ⅰ中盛放的试剂是浓硫酸,作用是干燥氯气
C. 装置Ⅲ的作用是便于控制通入NO2的量
D. 若制备的NO2中含有NO,应将混合气体通入水中以除去NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V L NH3(已折算成标准状况下)通入1 L水中,形成密度为ρ g·cm-3的氨水,质量分数为w,其中含NH3的物质的量为a mol,下列说法正确的是
A.溶质的物质的量浓度c =![]() mol·L-1
mol·L-1
B.溶质的质量分数 w=![]() ×100%
×100%
C.溶液中c(OH-)= amol·L-1
D.上述溶液中再通入与原溶液等体积的水,所得溶液的质量分数大于0.5w
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能用勒夏特列原理来解释的是
A. 实验室采用排饱和食盐水的方法收集氯气Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
B. 工业上合成氨反应N2(g)+ 3H2 (g)![]() 2NH3(g) △H<0 选择500 ℃
2NH3(g) △H<0 选择500 ℃
C. H2、I2、HI平衡混合气体加压后颜色加深H2(g)+ I2(g)![]() 2HI(g)
2HI(g)
D. SO2氧化成SO3,往往需要使用催化剂2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A. 由图甲知,B点SO2的平衡浓度为0.3mol·L-1
B. 由图甲知,A点对应温度下的平衡常数为80
C. 达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示
D. 压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com