
【题目】下面两图均为原电池装置,有关说法错误的是( )
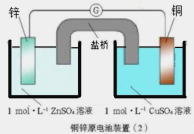
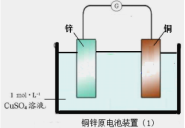
A.锌比铜活泼,锌为负极,发生氧化反应
B.电流从铜电极经导线流向锌电极
C.铜电极发生的反应为:Cu-2e-= Cu2+
D.装置(2)比装置(1)更能清楚揭示出电池中发生的化学反应
【答案】C
【解析】
根据装置图,锌比铜活泼,锌做负极,失电子,发生氧化反应;铜做正极,得电子,发生还原反应;电流从正极流向负极。电池总反应为:Zn+CuSO4=Cu+ ZnSO4
A. 原电池中,活泼电极做负极,锌比铜活泼,锌为负极,失电子,发生氧化反应,故A正确;
B. 原电池中电流从正极流向负极,根据上述分析,锌做负极,铜做正极,电流从铜电极经导线流向锌电极,故B正确;
C. 铜电极做正极,得电子,发生还原反应,反应为:Cu2++2e-= Cu,故C错误;
D. 装置(2)最大程度地避免了氧化剂与还原剂直接接触反应(非原电池反应),使反应尽可能实现通过外电路转移电子,装置(2)比装置(1)更能清楚揭示出电池中发生的化学反应,故D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】恒温条件下,可逆反应:2NO(g)+O2(g)![]() 2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2②单位时间内生成n mol O2的同时生成2n mol NO③用NO2、NO、O2表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的压强不再改变的状态⑦混合气体的平均相对分子质量不再改变的状态.
A. ①④⑥⑦ B. ②③⑤⑦ C. ①③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组以黄铜矿(主要成分CuFeS2)为原料进行如下实验探究.为测定黄铜矿中硫元素的质量分数,将m1g该黄铜矿样品放入如图所示装置中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铜矿样品.

(1)锥形瓶A内所盛试剂是__________;装置B的作用是__________;锥形瓶D内发生反应的离子方程式为__________。
(2)反应结束后将锥形瓶D中的溶液进行如下处理:

如图则向锥形瓶D中加入过量H2O2溶液反应的离子方程式为__________;操作Ⅱ是洗涤、烘干、称重,其中洗涤的具体方法__________;该黄铜矿中硫元素的质量分数为__________(用含m1、m2的代数式表示).
(3)反应后固体经熔炼、煅烧后得到泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO),要验证熔渣中存在FeO,应选用的最佳试剂是__________
A.KSCN溶液、氯水B.稀盐酸、KMnO4溶液
C.稀硫酸、KMnO4溶液D.NaOH溶液
(4)已知:Cu+在强酸性环境中会发生反应生成Cu和Cu2+.设计实验方案验证泡铜中是否含有Cu2O__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室要用18mol/L 浓硫酸配制100 mL 3.0mol/L 稀硫酸,请回答下列问题:
(1)所需浓硫酸的体积是________;量取浓硫酸所用的量筒的规格是_________(填选项代号)
A. 10mL B. 20mL C. 50mL D. 100mL
(2)实验操作步骤为:
A.把制得的溶液小心地转移至容量瓶中。
B.量取所需浓硫酸 ,在烧杯中用适量的蒸馏水将它稀释并冷却至室温。
C.继续向容量瓶中加蒸馏水至液面距刻度1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E.将容量瓶塞塞紧,充分摇匀。
操作步骤的正确顺序为___________________(填序号)。
(3)下列情况中,会使所配溶液浓度偏高的是___________(填序号)。
A.量取所需浓硫酸某同学观察液面时仰视
B.没有进行上述的操作步骤D
C.加蒸馏水时,不慎超过了刻度线
D.容量瓶使用前内壁沾有水珠
E.用少量蒸馏水洗涤量取浓硫酸后的量筒,洗涤的液体注入容量瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙_____;B________; G_______。
(2)写出反应②反应的化学方程式:_______;反应③的离子方程式:________。
(3)反应①-④的4个反应属于氧化还原反应的有_________ (填选项代号)
A.①②③④ B.①②③ C.①②③ D.①③④
(4)0.1mol的金属单质A与一定量的水完全反应,可得到标准状况下的甲气体_____ L,若得到的D溶液体积为100mL,则溶液的物质的量浓度为___________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室用自来水制取蒸馏水的实验中,下列说法正确的是( )
A.蒸馏烧瓶中加满自来水并放入几粒沸石
B.冷凝水应该是下进上出,与蒸气的流向相反
C.开始蒸馏时,应该先加热,再通冷凝水
D.蒸馏完毕时,应该先停止通冷凝水再撤酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外活动小组以海带为原料获得少量碘水,并以四氯化碳(沸点76.80C)为溶剂将碘从碘水中提取出来,具体过程如图所示。

请回答下列问题:
(1)操作①的名称为________________、_________________;
(2)向含碘单质的水溶液中加入CCl4振荡、静置后,观察到的现象是______________________;
(3)操作③中,将含碘单质的水溶液与CCl4在分液漏斗中混合、振荡摇匀放在铁架台的铁圈上,分液漏斗的下端尖嘴处紧贴在承接的烧杯内壁上静置后,下面的操作步骤是_______________________。
(4)从含碘的有机溶剂中经过蒸馏可以提取碘和回收有机溶剂,该实验需要的主要玻璃仪器除酒精灯、烧杯、温度计、锥形瓶、牛角管外,还需要____________________,实验中温度计水银球所处位置为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A. 常温常压下,11.2L二氧化硫所含的氧原子数等于NA
B. 0.5molH2O所含的电子数为9NA
C. 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA
D. 300mL2mol·L-1蔗糖溶液中所含分子数为0.6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com