
| A、1.0L 1.0 mol?L-1NaNO3溶液中含有的氧原子数为3NA |
| B、在标准状况下,22.4LCO2和O2混合气体中含有的氧原子数为NA |
C、 31 g P4 (分子结构如图)中含有的P-P键个数为1.5NA 31 g P4 (分子结构如图)中含有的P-P键个数为1.5NA |
| D、0.1mol Fe在0.1mol C12中充分燃烧,转移的电子数为0.3NA |
| 31g |
| 124g/mol |


科目:高中化学 来源: 题型:
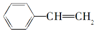
| A、易溶于水,不易溶于有机溶剂 |
| B、在空气中燃烧产生黑烟 |
| C、能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色 |
| D、能发生加成反应,在一定条件下可与4倍物质的量的氢气加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,下列说法正确的是( )
,下列说法正确的是( )| A、该元素位于第二周期第ⅡA族 |
| B、该元素位于第二周期第Ⅷ族 |
| C、该元素位于第三周期第ⅡA族 |
| D、该元素位于第三周期0族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铜丝放入氯化铁溶液中 |
| A、上述实验证明氧化性:Fe3+>Fe2+>Cu2+ |
| B、实验①中铁钉只作还原剂 |
| C、实验②中Fe2+既显氧化性又显还原性 |
| D、实验③中发生的是置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在配制FeCl2、FeCl3等溶液时,一般是将FeCl2、FeCl3等固体溶解在含少量HCl的溶液中,从而得到澄清的溶液 |
| B、除去CuCl2溶液中的Fe3+杂质时,通常是向其中加入CuO或Cu(OH)2等固体 |
| C、在一密闭容器中有一定量N2和H2,加入催化剂会使合成氨的速率加快 |
| D、常温下的醋酸溶液升温20℃,pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、防止硫酸铁分解 |
| B、抑制Fe2(SO4)3水解 |
| C、提高硫酸铁的溶解度 |
| D、提高溶液的pH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com