
| A. | 溶液的PH增大 | B. | 溶液中的Zn2+浓度增大 | ||
| C. | 溶液中的SO42- 浓度增大 | D. | 溶液的密度增大 |
分析 锌片-铜片-稀硫酸溶液组成的原电池中,较活泼的金属锌作负极,铜作正极;负极上锌失电子发生氧化反应,正极上氢离子得电子发生还原反应.
解答 解:A、原电池放电时,正极上氢离子得电子生成氢气析出,导致溶液中氢离子浓度降低,PH值增大,故A正确;
B、原电池放电时,负极上锌失电子生成锌离子进入溶液,导致溶液中锌离子浓度增大,故B正确;
C、原电池放电时,负极上锌失电子生成锌离子进入溶液,正极上氢离子得电子生成氢气,所以该反应中硫酸根离子浓度基本不变,故C错误;
D、原电池放电时,溶液由硫酸溶液逐渐变成硫酸锌溶液,所以溶液的密度增大,故D正确.
故选C.
点评 本题考查了原电池原理,难度不大,明确正负极上发生的电极反应是解本题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 该微粒不显电性 | |
| B. | 该微粒的质量数为2 | |
| C. | 在元素周期表中与氢元素占同一位置 | |
| D. | 它与普通中子互称同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:
如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ④
④ 等,其中C原子为sp2杂化的分子有①③④(填序号),预测HCHO分子的立体结构为平面三角形.
等,其中C原子为sp2杂化的分子有①③④(填序号),预测HCHO分子的立体结构为平面三角形.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 等浓度的H2CO3、Na2CO3溶液中c(HCO3-)前者小 | |
| B. | 反应HCO3-+H2O?H2CO3+OH-的平衡常数为10-5.37 | |
| C. | 1L0.1mol•L-1NaHC2O4溶液和1L0.1mol•L-1的NaOH溶液混合,混合液中c(HC2O4-)+c(C2O42-)+c(H2C2O4)=0.1mol•L-1 | |
| D. | Na2CO3溶液中加入过量草酸溶液,发生反应:CO32-+H2C2O4═HCO3-+HC2O4- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
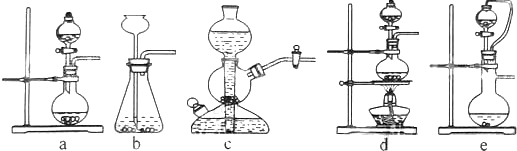
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl、CuCl2、Ba(OH)2 | B. | NaOH、CuSO4、H2SO4 | ||
| C. | Ba(OH)2、H2SO4、K2SO4 | D. | NaBr、H2SO4、Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
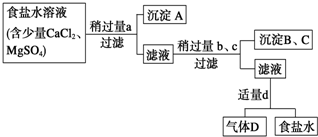

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com