(1)高温下,碳酸钠、碳酸钙分别和二氧化硅反应生成硅酸盐和二氧化碳,反应方程式分别为:Na
2CO
3+SiO
2 Na
2SiO
3+CO
2↑、CaCO
3+SiO
2CaSiO
3+CO
2↑,故答案为:Na
2CO
3+SiO
2 Na
2SiO
3+CO
2↑、CaCO
3+SiO
2CaSiO
3+CO
2↑;
(2)氢氧化亚铁不稳定,易被氧化生成氢氧化铁,反应方程式为:4Fe(OH)
2+O
2+2H
2O=4Fe(OH)
3,故答案为:4Fe(OH)
2+O
2+2H
2O=4Fe(OH)
3;
(3)Al和水不反应,所以剩余金属应该是Al,反应方程式为2Na+2H
2O=2NaOH+H
2↑,2Al+2NaOH+2H
2O=2NaAlO
2+3H
2↑,可以得出关系式Na~NaOH~Al,则参与反应的Na和Al的质量之比为23:27,Na和Al的质量和为15g,所以n(Na)=
=0.3mol,n(Al)=
=0.3mol,根据Na、Al和氢气之间的关系式得氢气体积=(0.3mol×0.5+0.3mol×1.5)×22.4L/mol=13.44L,
故答案为:13.44;
(4)n(Al(OH)
3)=
=0.1mol<0.3mol,一种情况是:铝元素存在于偏铝酸钠和氢氧化铝中,
此时盐酸少量,只能沉淀一部分AlO
2-,根据NaAlO
2+HCl+H
2O=Al(OH)
3↓+NaCl得,n(HCl)=n(Al(OH)
3)=0.1mol,则盐酸体积=
=100mL;
另一种情况是铝元素存在于氯化铝和氢氧化铝中,此时盐酸较多,先把AlO
2-全部沉淀,后又将部分沉淀溶解,生成氢氧化铝需要n(HCl)=n(NaAlO
2)=n(Al(OH)
3)=0.3mol,溶解Al(OH)
3生成氯化铝需要盐酸的n(HCl)=3n(AlCl
3)=3×(0.3-0.1)mol=0.6mol,所以需要盐酸体积=
=900mL,
故答案为:100或900;
(5)固体混合物和稀硫酸反应后有固体剩余,说明溶液中不存在铁离子,向滤液中加入加入2mol/L的NaOH溶液,加至40mL时开始出现沉淀,说明硫酸有剩余,铁先和铜离子后和氢离子发生置换反应,所以滤液中的溶质是硫酸、硫酸亚铁,n(H
2SO
4)=2.2mol/L×0.12L=0.264mol,
与氢氧化钠反应的硫酸的物质的量=
n(NaOH)=
×2mol/L×0.04L=0.04mol,
剩余的硫酸的物质的量=0.264mol-0.04mol=0.224mol,
剩余硫酸与固体反应生成了硫酸亚铁,根据硫酸和硫酸亚铁的关系式计算硫酸亚铁的物质的量浓度=
=1.87mol/L,
故答案为:1.87.



 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案 (1)反应后生成铜多少克?
(1)反应后生成铜多少克? (2)加入铁粉前Fe2(SO4)3物质的量浓度。
(2)加入铁粉前Fe2(SO4)3物质的量浓度。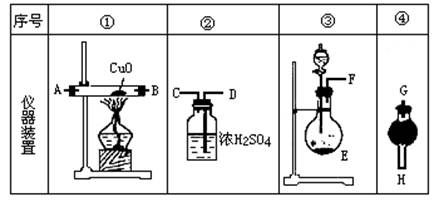

 ,
,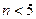 ,m<10}分批加入,利用PFS在水体中形成絮状物,以吸附镉离子。结合题中信息,下列说法不正确的是
,m<10}分批加入,利用PFS在水体中形成絮状物,以吸附镉离子。结合题中信息,下列说法不正确的是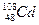 核素中中子数为60
核素中中子数为60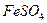 溶液制PFS需经过氧化、水解和聚合的过程
溶液制PFS需经过氧化、水解和聚合的过程