
| A.从海水中可以制取镁、溴、碘等物质 |
| B.电精炼铜(含少量Fe、Zn、Pt)的电解后溶液中,存在的金属阳离子只有Fe2+、Zn2+ |
| C.电解饱和食盐水可以制取烧碱、氯气、氢气 |
| D.在镀件上电镀铜,电镀过程中阳极减少的质量等于阴极增加的质量 |
科目:高中化学 来源:不详 题型:单选题
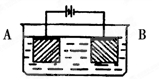
| A.4:1 | B.3:1 | C.2:1 | D.任意比 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
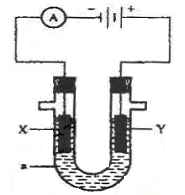
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
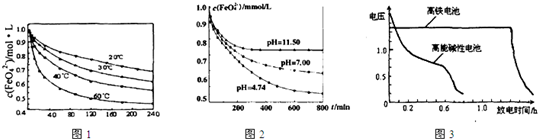
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
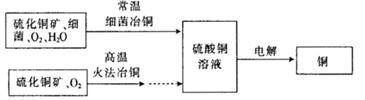
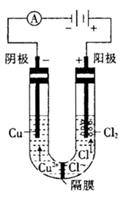
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
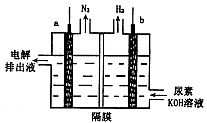
| A.电解时,b极是阴极放出H2,发生氧化反应 |
| B.溶液中OH—逐渐向b极移动 |
C.电解时,a极的电极反应式为: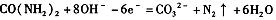 |
| D.若在b极产生标况下224mL氢气,则消耗尿素2g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解时,石墨作阴极,铁作阳极 |
| B.电解时,在阴极上产生KIO3 |
| C.电解后电解质溶液pH变大 |
| D.电解中每转移0.6mol e-,理论上可得到0.1mol无水KIO3晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
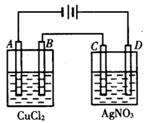
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.阴极只析出氢气 | B.阳极先析出氯气后析出氧气 |
| C.电解最后阶段为电解水 | D.电解过程中溶液的PH不断增大,最后pH为7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com