
图1-3
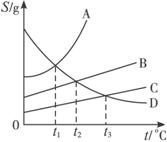
(1)当温度高于0 ℃低于t1 ℃时,四种物质溶解度由大到小的顺序是________。
(2)温度在________℃时,B、D两物质溶解度相等。
(3)随温度升高,D物质溶解度________。
(4)要想得到四种物质的晶体,A、B采取________方法,C采取________方法,D采取________方法,分离A、C可用________方法。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
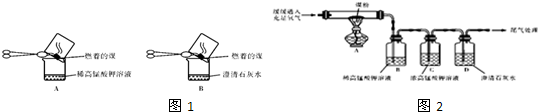
 某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素C和Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律,图2中A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素C和Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律,图2中A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
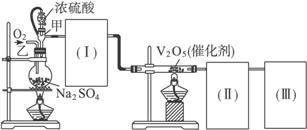
图1-3

图1-4
(1)根据实验的需要,(Ⅰ)(Ⅱ)(Ⅲ)处应连接合适的装置,从图1-4的A、B、C、D、E中选择合适的装置,将其序号填入以下空格内。(Ⅰ)(Ⅱ)(Ⅲ)所处连接的装置分别为____________________,____________________,____________________。
(2)实验时,浓硫酸能顺利地滴入烧瓶中,甲仪器起作用的原理是____________________。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时,在加热与滴加浓硫酸过程中,应采用的操作是____________________。
(4)用在火加热烧瓶时,SO2的转化率会____________________(填“提高”“不变”或“降低”)。
(5)用a mol粉末与足量浓硫酸进行此实验,当反应结束后,继续通入O2一段时间后,称得装置(Ⅲ)增重b g,则本实验中SO2的转化率为____________________。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江西省抚州市临川一中高一(下)月考化学试卷(3月份)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com