
现有一定量含有Na2O杂质的Na2O2试样,用如图所示的实验装置测定Na2O2试样的纯度.(可供选用的试剂只有CaCO3固体、6mol/L盐酸、6mol/L硫酸和蒸馏水)请回答下列问题:
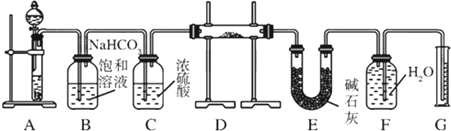
(1)装置A中的液体试剂选用 6 mol/L盐酸 ,理由是: 硫酸与CaCO3反应生成微溶的CaSO4,覆盖在CaCO3表面,使反应终止 ;
(2)装置B的作用是 除去气体中的HCl ,装置E中碱石灰的作用是: 吸收未反应的CO2 ;
(3)若开始时测得样品的质量为2.0g,反应结束后测得生成气体的体积为224mL(标准状况),计算出试样中Na2O2的纯度: 78% .
| 探究物质的组成或测量物质的含量. . | |
| 专题: | 实验探究和数据处理题. |
| 分析: | 由实验流程可知:A中用盐酸和碳酸钙反应生成二氧化碳气体,B中用于除杂,除去二氧化碳气体中的氯化氢,在C中干燥后通入D中,D中发生2Na2O2+2CO2=2Na2CO3+O2,Na2O+CO2=Na2CO3,E用于除去生成的氧气中的二氧化碳气体,然后用排水法测量氧气的体积,根据G中氧气的体积可知过氧化钠的质量,进而可确定Na2O2试样的纯度,以此解答该题. |
| 解答: | 解:(1)装置A是碳酸钙和盐酸反应生成二氧化碳,碳酸钙和硫酸反应时,生成的硫酸钙是微溶于水的,会覆盖在碳酸钙的表面,使反应不能持续,所以用盐酸而不用硫酸来反应, 故答案为:6 mol/L盐酸;硫酸与CaCO3反应生成微溶的CaSO4,覆盖在CaCO3表面,使反应终止; (2)碳酸钙和盐酸反应生成的二氧化碳气体中含有氯化氢气体,可以用饱和碳酸氢钠来除去,装置E中碱石灰的作用是吸收二氧化碳,防止对氧气的体积测量造成干扰, 故答案为:除去气体中的HCl;吸收未反应的CO2; (3)根据反应2Na2O2+2CO2=2Na2CO3+O2,反应结束后测得气体体积为224mL(标准状况),生成的氧气的物质的量为:n(O2)= 过氧化钠的纯度为:ω(Na2O2)= 故答案为:78%. |
| 点评: | 本题考查了探究过氧化钠中氧化钠的含量的方法,题目难度中等,试题综合性强,侧重对学生能力的培养和训练,有利于培养学生规范严谨的实验设计、操作能力,试题重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力. |


科目:高中化学 来源: 题型:
冰箱制冷剂氟氯甲烷在高空中受紫外线辐射产生Cl原子,并进行下列反应:Cl+O3→ClO+O2,ClO+O→Cl+O2下列说法不正确的是 ( )
A.反应后O3转变为O2 B.Cl原子是总反应的催化剂
C.氟氯甲烷是总反应的催化剂 D.Cl原子反复起分解O3的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
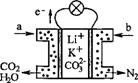 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见右图。下列说法正确的是
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见右图。下列说法正确的是
A.a为CH4,b为CO2
B.CO32﹣向正极移动
C.此电池在常温时也能工作
D.正极电极反应式为:O2+2CO2+4e﹣=2CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用固态不纯氯化钠(含少量NH4HCO3和Na2SO4杂质)制取纯净氯化钠溶液.下列操作可供选用:
①逐滴加入稀盐酸,调节pH值为5;
②煮沸;
③加蒸馏水溶解;
④加热至不再产生气体为止;
⑤加入稍过量的Na2CO3溶液;
⑥加入稍过量的BaCl2溶液;
⑦过滤.
上述实验操作的正确顺序应是( )
|
| A. | ①②⑤⑥⑦③④ | B. | ③④⑥⑤⑦①② | C. | ④③⑥⑤⑦①② | D. | ④③⑤⑥⑦②① |
查看答案和解析>>
科目:高中化学 来源: 题型:
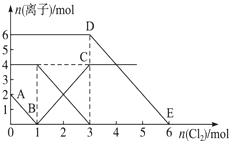
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.已知:Cl2+2Br﹣═2Cl﹣+Br2,2Fe2++Br2═2Fe3++2Br﹣,2Fe3++2I﹣═2Fe2++I2.则下列说法中不正确的是( )
|
| A. | 还原性:I﹣>Fe2+>Br﹣ |
|
| B. | 原混合溶液中FeBr2的物质的量为3mol |
|
| C. | 线段AB表示Fe2+被氯气氧化 |
|
| D. | 原溶液中:n(Fe2+):n(I﹣):n(Br﹣)═2:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:在100℃时,水的离子积为1×10-12,此时将pH=12的NaOH溶液V1 L与pH=l的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1∶V2为( )
A.1 : 9 B.10: 1 C.9 : 1 D.1: 10
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
| A.硫酸的摩尔质量是98g |
| B.铁原子的摩尔质量等于铁的相对原子质量 |
| C.标准状况下,任何物质的摩尔体积都约是22.4L |
| D.1mol氧气的质量为32g |
查看答案和解析>>
科目:高中化学 来源: 题型:
据考证,商代炼铜,主要矿物原料是孔雀石,主要燃料是木炭,冶炼温度估计在1000 ℃左右,可能涉及的反应有:①Cu2(OH)2CO3 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
②2CuO+C 2Cu+CO2↑
2Cu+CO2↑
③CuO+CO Cu+CO2
Cu+CO2
④CO2+C 2CO
2CO
(1)从四种基本反应类型看,①②④分别属于________、________、________。
(2)在上述反应中,属于氧化还原反应的是__________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1 ;②用物质B表示的反应的平均速率为0.6 mol·L
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1 ;②用物质B表示的反应的平均速率为0.6 mol·L -1·s-1;③2s时物质C的转化率为30% ;④2 s时物质B的浓度为0.7 mol·L-1。其中正确的是
-1·s-1;③2s时物质C的转化率为30% ;④2 s时物质B的浓度为0.7 mol·L-1。其中正确的是
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com