
| A、100 mL 1 mol?L-1的硫酸跟锌片反应,加入适量的硫酸钠溶液,反应速率不变 |
| B、SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢 |
| C、汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢 |
| D、用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 |


科目:高中化学 来源: 题型:
 金属在人类文明的发展进程中发挥了巨大作用,在人们已知的100多种元素中,金属元素约占80%,以下是关于金属的一些问题,请回答:
金属在人类文明的发展进程中发挥了巨大作用,在人们已知的100多种元素中,金属元素约占80%,以下是关于金属的一些问题,请回答:| 金属 | K | Cu |
| 原子半径/pm | 255 | 128 |
| 熔点/℃ | mp1 | mp2 |
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/℃ | 1266 | 1534 | 183 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①②④ |
| C、①②④⑤ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉和纤维素的化学式都是(C6H10O5)n,但由于n不同,淀粉和纤维素并不互为同分异构体 |
| B、鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可用灼烧的方法 |
| C、乙醇可以被酸性高锰酸钾溶液或酸性重铬酸钾溶液直接氧化成乙酸 |
| D、醇CH3CHOHCH3不能在铜或银作催化剂的条件下发生催化氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、少量BaCl2固体,v(H2)减小 |
| B、VmLNa2SO4溶液,v(H2)不变 |
| C、少量CuSO4溶液,v(H2)增大 |
| D、VmL稀硝酸,v(H2)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| A、该反应是焓变为负值 | |||
| B、其它条件不变,缩小容器体积,H2浓度一定增大 | |||
| C、升高温度,正反应速率增大,逆反应速率减小 | |||
D、该反应化学方程式为CO+H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
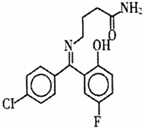 普罗加比对癫痫、痉挛和运动失调均有良好的治疗效果,其结构如图所示,有关普罗加比的说法正确的是( )
普罗加比对癫痫、痉挛和运动失调均有良好的治疗效果,其结构如图所示,有关普罗加比的说法正确的是( )| A、该分子在1H核磁共振谱中有12个峰 |
| B、一定条件下,1 mol普罗加比最多能与2 mol H2发生加成反应 |
| C、久置在空气中的普罗加比会因氧化而变质 |
| D、普罗加比可以和NaOH溶液、Na2CO3溶液反应,也可以和盐酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com