
| A、自来水 |
| B、0.5mol?L-1醋酸 |
| C、0.5mol?L-1硝酸 |
| D、0.5mol?L-1NaCl溶液 |


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
| A、已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| B、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ?mol--1,则氢气的燃烧热为241.8 kJ?mol-1 |
| C、已知2C(s)+2O2(g)═2CO2(g)△H=a 2C(s)+O2(g)═2CO(g)△H=b,则a>b |
| D、已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe分别与氯气和稀盐酸反应所得氯化物相同 |
| B、K、Zn分别与不足量的稀盐酸反应所得溶液均呈中性 |
| C、Li、Na、K的原子半径和密度随原子序数的增加而增加 |
| D、C、P、S、Cl的高价氧化物对应水化物的酸性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 环境要求 | 离子 |
| A | 溶液中c(K+)<c(Cl-) | K+、AlO2-、Cl-、NO3- |
| B | 溶液pH>7 | Na+、S2-、K+、ClO- |
| C | 水电离产生的c(H+)=10-12 mol/L的溶液 | ClO-、CO32-、NH4+、NO3-、SO32- |
| D | 向溶液中逐滴滴加烧碱溶液先有沉淀产生,后沉淀消失 | Na+、Al3+、Cl-、SO42- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
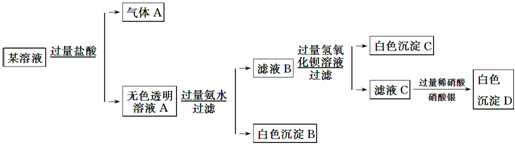
| A、原溶液中一定存在AlO2-、CO32-、SO42-、Cl-四种离子 |
B、气体A的化学式是CO2,其电子式为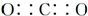 |
| C、原溶液中一定不存在的离子是Cu2+、Ba2+、Fe3+ |
| D、生成沉淀B的离子方程式为:Al3++3OH-=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、温度、容积不变时,通入SO2气体 |
| B、移走一部分NH4HS固体 |
| C、容积不变,充入氨气 |
| D、保持压强不变,充入氮气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28g乙烯所含共用电子对数目为4NA |
| B、0.5 mol1,3-丁二烯分子中含有C=C双键数为 NA |
| C、1 mol羟基所含的电子总数为9NA |
| D、标准状况下,11.2 L己烷所含分子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.01 mol?L-1的蔗糖溶液 |
| B、0.01 mol?L-1的CaCl2溶液 |
| C、0.02 mol?L-1的NaCl溶液 |
| D、0.02 mol?L-1的氨水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com