
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:下列说法不正确的是( )

A.固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B.捕获剂所捕获的气体主要是CO
C.X可以是空气,且需过量
D.处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-==N2↑+2H2O
【答案】C
【解析】
试题分析:工业废气中CO2、SO2可被石灰水吸收,生成固体1为CaCO3、CaSO3,气体1是不能被过量石灰水吸收的N2、NO、CO,气体1通入气体X,用氢氧化钠溶液处理后到的NaNO2,X可为空气,但不能过量,否则得到硝酸钠,NaNO2与含有NH4+的溶液反应生成无污染气体,应生成氮气,则气体2含有CO、N2,捕获剂所捕获的气体主要是CO。A.工业废气中CO2、SO2可被石灰水吸收,生成CaCO3、CaSO3,因氢氧化钙过量,则固体1为主要含有Ca(OH)2、CaCO3、CaSO3,故A正确;B.气体2含有CO、N2,经捕获剂得到氮气和CO,所捕获的气体主要是CO,防止污染空气,故B正确;C.由分析可知,气体1是不能被过量石灰水吸收的N2、NO、CO,气体1通入气体X,用氢氧化钠溶液处理后到的NaNO2,X可为空气,但不能过量,否则得到硝酸钠,故C错误;D.NaNO2与含有NH4+的溶液反应生成无污染气体,应生成氮气,发生氧化还原反应,离子方程式为NH4++NO2-=N2↑+2H2O,故D正确;故选C。


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,硫酸既表现出强氧化性,又表现出酸性的是( )
A.稀硫酸与锌粒反应生成气体
B.浓硫酸使铁、铝钝化
C.浓硫酸与铜反应加热反应产生SO2
D.浓硫酸和木炭在加热条件下反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的化学方程式或离子方程式,不正确的是( )
A.用FeSO4除去酸性废水中的Cr2O72-:Cr2O72-+6Fe2++14H+==2Cr3++6Fe3++7H2O
B.NH4Al(SO4)2溶液中加入少量的氢氧化钠溶液:Al3++3OH-==Al(OH)3↓
C.用惰性电极电解MgCl2溶液2H2O+2Cl-![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D.用CaSO4治理盐碱地:CaSO4(s)+Na2CO3(aq)![]() CaCO3(s)+Na2SO4(aq)
CaCO3(s)+Na2SO4(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,充入1mol N2 和3 mol H2,并在一定温度和压强条件下,使其发生反应:N2(g) + 3H2 (g) ![]() 2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol
(1)若保持容器体积不变,再向其中充入1mol N2,反应速率会_________(填“加快”、“减慢”或“不变”),理由是______________________。
(2)若保持容器体积不变,再向其中充入1mol氩气,反应速率会_________(填“加快”、“减慢”或“不变”),理由是_______________________。
(3)若保持容器气体压强不变,再向其中充入1mol N2 和3 mol H2,反应速率会_________(填“加快”、“减慢”或“不变”),理由是____________________。
(4)使用催化剂,反应速率会_________(填“加快”、“减慢”或“不变”),理由是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下物质的工业制备所用主要原料(括号内物质)不符合事实的是
A. 碘(海带) B. 溴(晒盐后的卤水) C. 乙烯(乙醇) D. 烧碱(氯化钠)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)完全燃烧一定质量的无水乙醇,放出的热量为QkJ,为完全吸收生成的CO2,并使之生成正盐,消耗0.8mol/L NaOH溶液50mL,则燃烧1mol酒精放出的热量是_________________。
(2)白磷与氧可发生如下反应:P4+5O2=P4O10。
已知断裂下列化学键需要吸收的能量分别为:
P-P akJ·mol-1、P-O bkJ·mol-1、
P=O ckJ·mol-1、O=O dkJ·mol-1
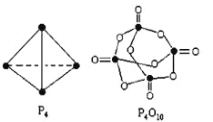
根据图示的分子结构和有关数据计算该反应的反应热__________________。
(3)现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=-19.4kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)0.5molN2的质量是,在标准状况下所占的体积约为,所含的原子数目约为。
(2)同温同压下,同质量的O2和O3,分子数之比为,原子数之比为,体积之比,密度之比为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于某无色溶液中所含离子的鉴别,下列判断正确的是 ( )
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在
B.通入Cl2后,溶液变为深黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在
C.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸后沉淀不溶解时,可确定有SO![]() 存在
存在
D.加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO![]() 存在
存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com