
| A�� | Cl2��I2��Co2O3��Fe3+ | B�� | Cl2��Co2O3��I2��Fe3+ | ||
| C�� | Co2O3��Cl2��Fe3+��I2 | D�� | I2��Fe3+��Cl2��Co2O3 |
���� ������ԭ��Ӧ�У��������������Դ�����������������ԣ����ݷ���ʽ��Ԫ�صĻ��ϼ۱仯�ж����������������
��� �⣺��Co2O3+6HCl��Ũ���T2CoCl2+Cl2��+3H2O�У���������Co2O3������������Cl2������������Co2O3��Cl2��
2FeCl3+2KI�T2FeCl2+2KCl+I2 ����������Fe3+������������I2������������Fe3+��I2��
2FeCl2+Cl2�T2FeCl3����������Cl2��������������Fe3+������������Cl2��Fe3+��
����������ǿ������˳���ǣ�Co2O3��Cl2��Fe3+��I2��
��ѡC��
���� ���⿼��������ǿ�����жϣ��ѶȲ���Ҫע����������ԭ��Ӧ�У���������������ǿ����������������ԣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������춡���һ��ȡ���ﶼֻ�����֣����ǵķе�Ҳ��ͬ | |
| B�� | ��ϩ�����뱽���Ӷ�����H2�����ӳɷ�Ӧ��˵�����߾���̼̼˫�� | |
| C�� | ���顢�����Ҵ������������������һ�������¶��ܷ���ȡ����Ӧ | |
| D�� | ��ȩ����Cu��OH��2��ĩ�����ȿɿ�����ɫ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2��ʹ����KMnO4��Һ��ɫ����CO2Ҳ��ʹ����KMnO4��Һ��ɫ | |
| B�� | ������þ��Ӧ������������������þ��ӦҲ�������� | |
| C�� | SO2��ʹƷ����Һ��ɫ����CO2Ҳ��ʹƷ����Һ��ɫ | |
| D�� | ������Ũ������ʹ�������ۻ����ʳ�����Ũ����Ҳ��ʹ�������ۻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ڢ� | C�� | �ڢۢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
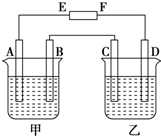 ��ͼ�У�E��F�ֱ�Ϊ��Դ���������ձ���ʢ��100mL 0.2mol•L-1 AgNO3��Һ�����ձ���ʢ��100mL 0.15mol•L-1 CuCl2��Һ��A��B��C��D��Ϊʯī�缫��������һ��ʱ�����B������1.08g����
��ͼ�У�E��F�ֱ�Ϊ��Դ���������ձ���ʢ��100mL 0.2mol•L-1 AgNO3��Һ�����ձ���ʢ��100mL 0.15mol•L-1 CuCl2��Һ��A��B��C��D��Ϊʯī�缫��������һ��ʱ�����B������1.08g�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Na2O2�м�������ˮ��2Na2O2+2H2O=4Na++4OH-+O2�� | |
| B�� | ��Ag��NH3��2NO3��Һ�м������Ag��NH3��2++2H+=Ag++2NH4+ | |
| C�� | ��Al2��SO4��3��Һ�м��������ˮ��Al3++3OH-=Al��OH��3�� | |
| D�� | ��Ca��HCO3��2��Һ�м������ʯ��ˮ��Ca2++2HCO3-+2OH-=CaCO3��+CO32-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.025 mol | B�� | 0.050 mol | C�� | 0.10 mol | D�� | 0.20 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com