
【题目】碘酸钾(![]() )在生活中应用广泛,可将含碘物质经过系列变化得到
)在生活中应用广泛,可将含碘物质经过系列变化得到![]() .现向含
.现向含![]() 的稀硫酸中逐漓加入
的稀硫酸中逐漓加入![]() 溶液,整个过程中含碘物质的物质的量与加入
溶液,整个过程中含碘物质的物质的量与加入![]() 的物质的量的关系如图所示。回答下列问题:
的物质的量的关系如图所示。回答下列问题:
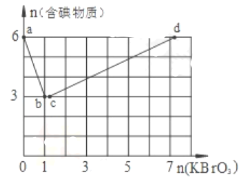
(1)已知![]() 段反应的离子方程式为
段反应的离子方程式为![]() b点时,KI恰好完全反应,则此时消耗的氧化剂与还原剂的物质的量之比是________还原产物是_______;共转移_______
b点时,KI恰好完全反应,则此时消耗的氧化剂与还原剂的物质的量之比是________还原产物是_______;共转移_______![]()
(2)![]() 过程中只有一种元素的化合价发生变化,写出该过程的离子方程式___________________从反应开始到达c点时,共消耗
过程中只有一种元素的化合价发生变化,写出该过程的离子方程式___________________从反应开始到达c点时,共消耗![]() ___________
___________![]()
【答案】1∶6 KBr 6 BrO3-+5Br-+6H+=3Br2+3H2O 1.2
【解析】
(1)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,根据I的物质的量变化规律可知该过程中I-被氧化成I2,KBrO3被还原成KBr,则KI为还原剂,KBrO3为氧化剂,则消耗的氧化剂与还原剂物质的量之比为1:6,还原产物是KBr,结合元素守恒和电子守恒可知a→b段反应方程式为:BrO3-+6I-+6H+=3I2+Br-+3H2O;1molKBrO3被还原成KBr,则转移6mol电子;
(2)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O;已知ab段发生反应BrO3-+6I-+6H+=3I2+Br-+3H2O,消耗KBrO3为1mol,则生成的Br-为1mol,根据bc段反应BrO3-+5Br-+6H+=3Br2+3H2O可知该段消耗KBrO3为0.2mol,则从反应开始到达c点时,共消耗n(KBrO3)=1mol+0.2mol=1.2mol。


科目:高中化学 来源: 题型:
【题目】实验室模拟合成氨和氨催化氧化的流程如下:

已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从如图中选择制取气体的合适装置:氮气________、氢气________。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有________、________。

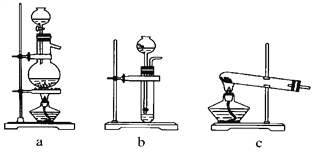
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,________(“会”或“不会”)发生倒吸,原因是_________________。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是________,锥形瓶中还可观察到的现象是____________________________。
(5)写出乙装置中氨氧化的化学方程式:_____________________________________________。
(6)反应结束后锥形瓶内的溶液含有H+、OH-、______、________离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮、氟、硅、铜等元素的化合物广泛存在于自然界,回答下列问题:
(1)基态氟原子核外电子的电子云形状有_____种;氟原子的价电子排布式为___。
(2)NF3是微电子工业中优良的等离子刻蚀气体,NF3分子的空间构型为______;写出与N2互为等电子体的一种离子的化学式_______。
(3)已知金刚石中的C-C键键长为154.45pm,C60中C-C键键长为145~140pm,而金刚石的熔点远远高于C60,其理由是________。
(4)氢基倍半硅氧烷的分子结构如图所示,该分子的分子式为______,Si原子采用_______杂化。
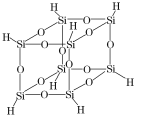
(5)Cu的某种晶体晶胞为面心立方结构,晶胞边长为acm,原子的半径为rcm。该晶体中铜原子的堆积方式为_______(填“A1”“A2”或“A3”),该晶体的密度为______g/cm3(用含a和NA的代数式表示),该晶体中铜原子的空间利用率为______(用含a和r的代数式表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E、G的原子序数依次增大,在元素周期表中A的原子半径最小(稀有气体元素除外),B与C相邻且C的最外层电子数是次外层的3倍,C、D的最外层电子数之和与G的最外层电子数相等,E是地壳中含量最多的金属元素。回答下列问题:
(1)C在元素周期表中的位置是__________;由C和D组成既含离子键又含共价键的化合物的电子式__________。
(2)分别由C、D、E、G元素形成的简单离子的半径由大到小的顺序为__________(用相应的离子符号表示)。
(3)写出实验室中制备G元素的单质的离子方程式______________________________
(4)E单质能写D的最高价氧化物的水化物浓溶液反应放出氢气,反应的离子方程式是:__________由上述六种元素中的三种组成的某种盐,是漂白液的主要成分,将该盐溶液滴入硫酸酸化的KI淀粉溶液中,溶液变为蓝色,则反应的化学方程式为________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求填空
①![]() 的名称为:_________;
的名称为:_________;
②苯酚与浓溴水反应的化学方程式:________________________;
③某有机物A的相对分子质量为74,且红外光谱图如图,则A的结构简式为____________。
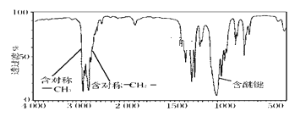
④物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈__性,醋酸体积__氢氧化钠溶液体积。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨基苯甲酸可用甲苯为原料合成,已知苯环上的硝基可被还原为氨基:![]() +3Fe+6HCl→
+3Fe+6HCl→![]() +3FeCl2+2H2O,产物苯胺还原性强,易被氧化,则由甲苯合成对氨基苯甲酸的步骤合理的是( )
+3FeCl2+2H2O,产物苯胺还原性强,易被氧化,则由甲苯合成对氨基苯甲酸的步骤合理的是( )
已知:—CH3为邻、对位取代定位基;而—COOH为间位取代定位基
A.甲苯![]() X
X![]() Y
Y![]() 对氨基苯甲酸
对氨基苯甲酸
B.甲苯![]() X
X![]() Y
Y![]() 对氨基苯甲酸
对氨基苯甲酸
C.甲苯![]() X
X![]() Y
Y![]() 对氨基苯甲酸
对氨基苯甲酸
D.甲苯![]() X
X![]() Y
Y![]() 对氨基苯甲酸
对氨基苯甲酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应C(s)+H2O(g)![]() CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动 ②已达平衡的反应N2(g)+3H2(g)
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动 ②已达平衡的反应N2(g)+3H2(g)![]() 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高 ③有气体参加的反应达到平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动 ④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高 ③有气体参加的反应达到平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动 ④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
A.①④B.①②③C.②③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在容积固定不变的密闭容器中进行如下可逆反应:X(g)+Y(g)![]() Z(g)+W(s)-Q,一段时间后,达到化学平衡状态.下列叙述正确的是
Z(g)+W(s)-Q,一段时间后,达到化学平衡状态.下列叙述正确的是
A.加入少量W,逆反应速率增大
B.通入一定量氦气,压强增大,平衡向正反应方向移动
C.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
D.降低温度,正反应速率减小,逆反应速率也减小,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容的密闭容器中充入2molA和1molB的气体后发生反应2A(g)+B(g)xC(g),达到平衡后,C的体积分数为m%。若维持容器容积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质的量,达到平衡后,C的体积分数仍为m%。则x的值可能为( )
A.1 或2B.2 或3C.3 或4D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com