
【题目】在含有Cu(NO3)2、Mg(NO3)2、AgNO3的溶液中加入适量锌粉,首先置换出的是( )
A.Mg B.Cu C.Ag D.H2
科目:高中化学 来源: 题型:
【题目】已知拆开1mol氢气中化学键需要吸收436kJ热量,拆开1mol氧气中的化学键需要吸收496kJ的热量,形成1molH—O共价键放出463kJ的热量。反应2H2(g)+O2(g)=2H2O(g)的能量变化如右图所示。下列说法正确的是

A. 2H(g)→H2(g) ![]() H >0
H >0
B. 图中E1 = 932kJ
C. 图中E2 = 926 kJ
D. 2H2(g)+O2(g)=2H2O(g) ![]() H =-484 kJ·mol-1
H =-484 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某药物H的合成路线如下图所示,试回答下列问题:
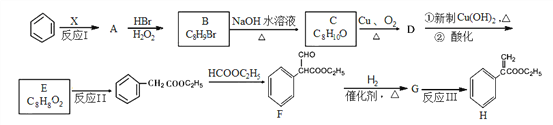
(1)反应Ⅰ中X为烃,其氢的质量分数与苯相同,则X的名称______________。
(2)写结构简式:A__________。D_____________。
(3)写出反应Ⅱ的反应条件:_________________。
(4)写出反应类型:A→B__________。C→D__________。
(5)写出G→H的化学反应方程式:________________________________________。
(6)写出两种满足下列条件的E的同分异构体的结构简式:____________、___________。
①发生银镜反应 ②苯环上有2个取代基 ③属于不同类别的有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑(未配平)
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外未成对电子数是______个;
O2—、Na+、Cl—中半径最小的是_____________。
(2)NaCN晶体中含有的化学键类型为___________________。
(3)第二段过程中,产物属于共价化合物的电子式是___________,其属于__________(填“极性”或“非极性”)分子。
(4)已知:NaOCN中N元素为-3价。配平第二段过程的化学方程式并标出电子转移的方向和数目。_______________
(5)综合两段反应,处理含有0.01 mol NaCN的废水,至少需NaClO________mol。
(6)请用一个方程式证明氮的非金属性大于碳:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)===Na2CO3(s)+![]() O2(g) ΔH=-226 kJ·mol-1
O2(g) ΔH=-226 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是( )
A. CO的燃烧热为283 kJ
B. 下图可表示由CO生成CO2的反应过程和能量关系
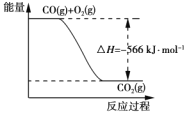
C. 2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-452 kJ·mol-1
D. CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ和Ⅱ中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )
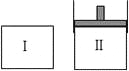
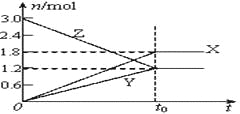
A. 该反应的化学方程式为:3X+2Y![]() 2Z
2Z
B. 若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0
C. 若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态
D. 若达平衡后,对容器Ⅱ升高温度时,其体积增大,说明Z发生的反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种生产碘的方法是用亚硫酸氢钠还原碘酸盐(IO3-),每还原出1mol碘分子,理论上需用去亚硫酸氢钠( )
A. 1mol B. 2mol C. 2.5mol D. 5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com