
【题目】(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质 A 可以是_____(填序号,下同),其中①~⑧中的电解质有_____。
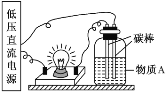
①干燥的氯化钠晶体 ②干燥的氢氧化钠固体 ③蔗糖晶体 ④酒精 ⑤NaHSO4 溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧Ba(OH)2 溶液
(2)向盛有⑧的溶液中,逐滴加入⑤,当溶液中的Ba2+恰好完全沉淀时,发生反应的离子 方程式为_________。
(3)某无色透明溶液中可能含有下列离子中的一种或几种:Na+、Mg2+、Cu2+、OH-、Cl-、CO32-、NO3-。现进行如下实验:
①用红色石蕊试纸检验,试纸变蓝色。
②另取少量溶液逐滴滴加盐酸至过量,无气体放出,再加入 BaCl2 溶液后,没有沉淀生成。
③另取少量溶液用硝酸酸化后,加入 AgNO3 溶液有白色沉淀生成。 根据上述实验推断:原溶液中肯定有__________离子,肯定没有_____离子。
【答案】⑤⑥⑦⑧ ①② Ba2++OH-+H++SO42-=BaSO4↓+H2O OH-、Na+、Cl- Mg2+、Cu2+、CO32-
【解析】
(1)若灯泡亮,说明物质A中含有大量自由移动的离子;对照电解质的概念分析,据以上分析进行解答;
(2)向⑧Ba(OH)2 溶液逐滴加入⑤NaHSO4 溶液,当溶液中的 Ba2+恰好完全沉淀时,反应生成硫酸钡、氢氧化钠和水,据此写出反应的离子方程式;
(3)由题干“无色溶液”排除Cu2+(蓝色)的存在;由实验①知有OH-的存在,无Mg2+;由实验②知无CO32-;由实验③知有Cl-的存在。根据电荷守恒,溶液中有Na+存在。整个实验过程中,NO3-不影响实验的过程,故不能确定NO3-是有还是无。
(1)若灯泡亮,说明物质A中含有大量自由移动的离子,⑤氯化钠溶液、⑥氢氧化钠溶液、⑦稀盐酸、 ⑧硫酸铜溶液中都含有大量自由移动的离子,所以能导电,剩余几种物质中都不含有自由移动的离子,所以不能导电,故选⑤⑥⑦⑧;溶于水或熔融状态下能导电的化合物是电解质,而⑤⑥⑦⑧均为混合物,③ ④均为非电解质,因此只有①干燥的氯化钠晶体和②干燥的氢氧化钠固体属于电解质;
故答案是:⑤⑥⑦⑧;①②;
(2)向⑧Ba(OH)2 溶液逐滴加入⑤NaHSO4 溶液,当溶液中的 Ba2+恰好完全沉淀时,反应生成硫酸钡、氢氧化钠和水,发生反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O;
故答案为:Ba2++OH-+H++SO42-=BaSO4↓+H2O;
(3)无色透明溶液,排除Cu2+的存在;用红色石蕊试纸检验变蓝,一定有氢氧根离子,所以一定没有铜离子、镁离子,根据电荷守恒规律可知一定有钠离子;另取少量溶液加盐酸至过量,无气体放出;加BaCl2溶液无沉淀,一定没有碳酸根离子;另取少量溶液用硝酸酸化后,加硝酸银有白色沉淀生成,所以一定有氯离子;硝酸根离子无法确定是否存在;因此原溶液中肯定有OH-、Na+、Cl-;肯定没有Mg2+、Cu2+、CO32-;
故答案是:OH-、Na+、Cl- ; Mg2+、Cu2+、CO32-。


科目:高中化学 来源: 题型:
【题目】化学上通常把原子数和电子数相等的分子或离子称为等电子体,研究发现等电子体间结构和性质相似(等电子原理).化合物B3N3H6被称为无机苯,它与苯是等电子体,则下列说法中不正确的是( )
A. 无机苯是仅由极性键组成的分子
B. 无机苯能发生取代反应
C. 无机苯的二氯代物有3种同分异构体
D. 无机苯不能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用以下流程从铜沉淀渣中回收铜、硒、碲等物质。沉淀渣中除含有铜![]() 、硒
、硒![]() 、碲
、碲![]() 外,还含有少量稀贵金属,主要物质为
外,还含有少量稀贵金属,主要物质为![]() 、
、![]() 和
和![]() 。
。
(1)![]() 、
、![]() 、
、![]() 为同主族元素,其中
为同主族元素,其中![]() 在元素周期表中的位置____。
在元素周期表中的位置____。
其中铜、硒、碲的主要回收流程如图:

(2)经过硫酸化焙烧,铜、硒化铜和碲化铜转变为硫酸铜。
①写出![]() 硫酸化焙烧的化学方程式____。
硫酸化焙烧的化学方程式____。
②“水浸固体”过程中补充少量氯化钠固体,可减少固体中的银(硫酸银)进入浸出液中,结合化学用语,从平衡移动原理角度解释其原因___。
③滤液2经过____、_____、过滤、洗涤、干燥可以得到硫酸铜晶体。
(3)所得粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示。蒸馏操作中控制的最佳温度是____(填序号)。

a.455℃ b.462℃ c.475℃ d.515℃
(4)目前碲化镉薄膜太阳能行业发展迅速,被认为是最有发展前景的太阳能技术之一。用如下装置可以完成碲的电解精炼。研究发现在低的电流密度、碱性条件下,随着![]() 浓度的增加,促进了
浓度的增加,促进了![]() 的沉积。写出
的沉积。写出![]() 的沉积的电极反应式为____。
的沉积的电极反应式为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯氧布洛芬钙G是评价较好的解热、镇痛、消炎药,如图是它的一种合成路线(具体反应条件和部分试剂略)

已知:
①氯化亚砜![]() 可与醇发生反应,醇的羟基被氯原子取代而生成氯代烃。
可与醇发生反应,醇的羟基被氯原子取代而生成氯代烃。
② +X2
+X2 +HX(X表示卤素原子)
+HX(X表示卤素原子)
③![]()
回答下列问题:
(1)F中所含的官能团名称是_______。
(2)![]() 的反应类型是______。
的反应类型是______。
(3)写出F和C在浓硫酸条件下反应的化学方程式______。
(4)写出A的符合以下条件同分异构体的所有结构简式_______。
①属于苯的二取代物; ②苯环上的一氯代物有2种; ③与![]() 溶液发生显色反应。
溶液发生显色反应。
(5)结合上述推断及所学知识,参照上述合成路线任选无机试剂设计合理的方案,以苯甲醇(![]() )为原料合成苯乙酸苯甲酯(
)为原料合成苯乙酸苯甲酯(![]() )写出合成路线,并注明反应条件____。
)写出合成路线,并注明反应条件____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于乙醇 在化学反应中断键位置说法错误的是 ( )
在化学反应中断键位置说法错误的是 ( )
A. 乙醇与浓硫酸在170℃时,在②③位置断裂,以水分子的形式消去,属于消去反应。
B. 乙醇与钠反应,在④位置断裂,对比钠与水反应,乙醇比水更难失去氢离子。
C. 乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应属于取代反应。
D. 乙醇在铜催化下与氧气反应,在②④位置断裂,所以只有与羟基直接相连的碳原子上有氢原子才能发生催化氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用乙醇制取乙烯的装置如下图,回答下列问题。

(1)仪器A的名称是__________ ;A中加入沸石的目的是 __________;在烧杯中配制A中溶液的方法是__________ ;在反应中浓硫酸的作用是__________;A中发生反应的化学方程式是 __________ 。
(2)A中产生的气体除乙烯外,还可能混有少量 __________(填化学式)
(3)用乙烯制聚乙烯的化学方程式为 __________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若以NA代表阿伏加德罗常数的值,下列说法中正确的是
A.20g NaOH溶于1L水,可配得0.5mol/LNaOH溶液
B.100mL 0.1mol/L硫酸溶液中含有的氧原子数约为0.04NA
C.5 mL 0.3 mol/L Na2SO4溶液和5 mL 0.3 mol/L NaNO3溶液Na+ 物质的量浓度相等
D.a g C2H4和C3H6的混合物所含碳原子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图表示的一些物质或概念间的从属关系中不正确的是

X | Y | Z | |
A | 酸 | 电解质 | 化合物 |
B | 酸式盐 | 盐 | 化合物 |
C | 溶液 | 分散系 | 物质 |
D | 置换反应 | 氧化还原反应 | 离子反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
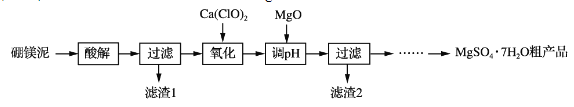
【题目】实验室用硼镁泥为原料制取MgSO4·7H2O粗产品的过程如下:
硼镁泥的主要成分如下表:
MgO | SiO2 | FeO、Fe2O3 | CaO | Al2O3 | B2O3 |
30%~40% | 20%~25% | 5%~15% | 2%~3% | 1%~2% | 1%~2% |
(1)“酸解”时为提高Mg2+的浸出率,可采用的措施是_____(写一种)。所加酸不宜过量太多的原因是_____。
(2)“氧化”步骤中,若用H2O2代替Ca(ClO)2,则发生反应的离子方程式为______________。实际未使用H2O2,除H2O2成本高外,还可能的原因是______________________________________。
(3)“调pH”时用MgO而不用NaOH溶液的原因是________________________。
(4)结合附表信息,由MgSO4·7H2O粗产品(含少量CaSO4)提纯获取MgSO4·7H2O的实验方案如下:将粗产品溶于水,_________________________________________________,室温下自然挥发干燥。(实验中必须使用的试剂有:饱和MgSO4溶液,乙醇)附:两种盐的溶解度(g/100 g水)
温度℃ | 10 | 30 | 40 | 50 |
CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 |
MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com