
镁、铝都是较活泼的金属,下列描述中正确的是 ( )
A.铝的导电性比铜、银更强,所以常用以制造电线、电缆
B.镁、铝都能跟稀盐酸、稀硫酸、强碱反应
C.镁在点燃条件下可以与二氧化碳反应,铝在一定条件下可以与氧化铁发生氧化还原反应
D.铝热剂是镁条、铝粉和氧化铁的混合物
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
下列溶液中各微粒浓度关系判定不正确的是
A.10mL 0.2 mol·L-1的氨水与l0mL 0.1 mol·L-1的盐酸充分反应混合后的溶液中,存在
c(NH4+)+c(NH3·H2O)=2c(Cl-)= 0.1 mol·L-1
B.已知酸性HF > CH3COOH,物质的量浓度相等的NaF与CH3COOK溶液中:
c(Na+) - c(F-) > c(K+) - c(CH3COO-)
C.CH3COOK溶液中加入少量NaNO3固体后的碱性溶液一定有:
c(K+) + c(H+) = c(CH3COO-) + c(OH-)
D.NaHSO3溶液中一定有:c(Na+)> c(HSO3-)> c(SO32-)>c(H2SO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E属于短周期元素,原子序数依次增大,已知A 与E同主族,B、C、D、E同周期,A与B可形成两种离子化合物甲和乙,在甲中A、B 离子的电子层结构相同;C的简单离子半径是同周期所有离子中最小的,高纯度的D单质可制造芯片;又知 C、D的单质都能与强碱溶液反应。
A、B、C、D、E属于短周期元素,原子序数依次增大,已知A 与E同主族,B、C、D、E同周期,A与B可形成两种离子化合物甲和乙,在甲中A、B 离子的电子层结构相同;C的简单离子半径是同周期所有离子中最小的,高纯度的D单质可制造芯片;又知 C、D的单质都能与强碱溶液反应。
(1)写出: A D (元素符号),乙 (化学式)。
(2)E元素在周期表中的位置是第 周期,第 族。
(3)画出B的原子结构示意图 ;
(4)C单质与NaOH溶液反应的离子方程式 ;
(5)举出C单质在工业上的一种重要用途(必须用化学方程式表示) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关晶体的结构如图所示,下列说法中不正确的是 ( )
A.在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体
B.该气态团簇分子(图乙)的分子式为E4F4或F4E4
C.在SiO2晶体(图丙)中,1molSi原子最多可形成4molSi-O键
D.单质锌采取六方最密堆积(图丁),配位数为8

甲 乙 丙 丁
查看答案和解析>>
科目:高中化学 来源: 题型:
某金属晶体M有两种堆积形式,如下图甲和乙,在T℃以上时甲可以转变为乙,这两种结构中最邻近的原子间距离相同。

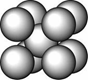
甲 乙
(1)乙的堆积方式称为 堆积;
甲和乙两种堆积方式中配位数之比为 ,晶胞边长之比为 。
(2)在T℃以下测定该金属晶体有关性质参数如下表所示。已知原子化热指1mol金属由固态转变为气态原子时所需要吸收的热量,是衡量金属键强弱的物理量。
| 金属 | 相对原子质量 | 密度/g·㎝-3 | 原子化热/kJ·mol-1 |
| Na | 22. 99 | 0. 960 | 108. 4 |
| M | 60. 20 | 7. 407 | 7735 |
预测该金属的熔点比Na (填“高”或“低”),由上述数据可计算M原子的原子半径为 pm。
(已知 ,7. 407≈
,7. 407≈ ,1pm=10
,1pm=10 m)
m)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是 ( )
①NaHCO3 ②(NH4)2SO3 ③Al2O3 ④Al(OH)3 ⑤Al
A.全部 B.只有①③④⑤
C.只有③④⑤ D.只有②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为长式周期表的一部分,其中的编号代表对应的元素。
| ① | ② | ||||||||||||||||
| ③ | ④ | ⑤ | |||||||||||||||
| ⑦ | ⑥ |
请回答下列问题:
(1) ①和⑤形成的一种常见溶剂的电子式为
(2) 元素⑦的基态原子的简化电子排布式为
(3) ②的氢化物与⑤的氢化物比较,沸点②的更高,热稳定性②的也更强。请分别说明理由: ;
 (4) 右图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物的沸点变化,则④的氢化物所在的折线是 (填m、n、x或y)。
(4) 右图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物的沸点变化,则④的氢化物所在的折线是 (填m、n、x或y)。
(5)③与⑤构成的晶体晶胞如下图所示。已知晶体的密度为r g / cm3,阿伏加德罗常数为NA,则在晶体里距离最近的离子③与⑤的间距大约是 cm. (列出算式即可,不必化简)

(6)元素⑥的单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

若元素⑥ 的原子半径为r cm,NA代表阿伏加德罗常数,则该晶体的密度可表示为
g / cm3。(列出算式即可,不必化简)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com