
某金属晶体M有两种堆积形式,如下图甲和乙,在T℃以上时甲可以转变为乙,这两种结构中最邻近的原子间距离相同。

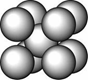
甲 乙
(1)乙的堆积方式称为 堆积;
甲和乙两种堆积方式中配位数之比为 ,晶胞边长之比为 。
(2)在T℃以下测定该金属晶体有关性质参数如下表所示。已知原子化热指1mol金属由固态转变为气态原子时所需要吸收的热量,是衡量金属键强弱的物理量。
| 金属 | 相对原子质量 | 密度/g·㎝-3 | 原子化热/kJ·mol-1 |
| Na | 22. 99 | 0. 960 | 108. 4 |
| M | 60. 20 | 7. 407 | 7735 |
预测该金属的熔点比Na (填“高”或“低”),由上述数据可计算M原子的原子半径为 pm。
(已知 ,7. 407≈
,7. 407≈ ,1pm=10
,1pm=10 m)
m)
科目:高中化学 来源: 题型:
在恒容密闭容器中存在下列平衡:


 。
。 的平衡物质的量浓度
的平衡物质的量浓度 与温度T的关系如右图所示。下列说法错误的是
与温度T的关系如右图所示。下列说法错误的是
A.反应

 的
的
B.在 时,若反应处于状态
时,若反应处于状态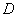 ,则一定有v(逆)>v(正)
,则一定有v(逆)>v(正)
C.平衡状态 与
与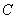 相比,平衡状态
相比,平衡状态 的
的 小
小
D.若 时的平衡常数分别为
时的平衡常数分别为 ,则
,则

查看答案和解析>>
科目:高中化学 来源: 题型:
230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是
A. Th 元素的质量数是232 B. Th 元素的相对原子质量是231
C. 230Th和232Th的性质相同 D. 230Th和232Th的化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.C2H4和HCN分子中,都含σ键和π键,但C原子的杂化方式并不相同
B.在元素周期表中,p区元素的最外层电子排布均可表示为ns2np1~6
C.某基态原子的核外电子排布图为 ,它违背了泡利不相容原理
,它违背了泡利不相容原理
D.用红外光谱可鉴别乙醇和二甲醚,用X-射线衍射实验可鉴别玻璃与水晶
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)
(1) 的名称是
的名称是
(2)写出右图化合物A中含氧官能团的名称
(3)某物质的实验式是Co(NH3)5BrSO4,向它的溶液中加入BaCl2溶液时,无明显现象;加入强碱处理,也无气体放出。若加入 AgNO3溶液时,产生淡黄色沉淀。写出它的配位化学式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
镁、铝都是较活泼的金属,下列描述中正确的是 ( )
A.铝的导电性比铜、银更强,所以常用以制造电线、电缆
B.镁、铝都能跟稀盐酸、稀硫酸、强碱反应
C.镁在点燃条件下可以与二氧化碳反应,铝在一定条件下可以与氧化铁发生氧化还原反应
D.铝热剂是镁条、铝粉和氧化铁的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
已知室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3。向浓度均为0.1 mol·L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积的关系,合理的是 ( )


查看答案和解析>>
科目:高中化学 来源: 题型:
已知2H2(g)+O2(g)===2H2O(l);ΔH=-569.6 kJ·mol-1,
2H2O(g)===2H2(g)+O2(g);ΔH=+482.1 kJ·mol-1。
则1 g液态H2O蒸发时吸收的热量是( )
A.2.43 kJ B.4.86 kJ C.43.8 kJ D.87.5 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com