
在恒容密闭容器中存在下列平衡:


 。
。 的平衡物质的量浓度
的平衡物质的量浓度 与温度T的关系如右图所示。下列说法错误的是
与温度T的关系如右图所示。下列说法错误的是
A.反应

 的
的
B.在 时,若反应处于状态
时,若反应处于状态 ,则一定有v(逆)>v(正)
,则一定有v(逆)>v(正)
C.平衡状态 与
与 相比,平衡状态
相比,平衡状态 的
的 小
小
D.若 时的平衡常数分别为
时的平衡常数分别为 ,则
,则

科目:高中化学 来源: 题型:
5种有机物:①乙烯 ,②乙醇,③乙醛,④乙酸,⑤乙酸乙酯。
(1)请分别写出其中含有下列官能团的有机物的结构简式
①-OH________ ②-CHO________ ③-COOH________
(2)在上述5种有机物中(填写序号)
①能发生银镜反应的是 。
②能发生水解反应的是
③具有酸性且能发生酯化反应的是
④既能发生加成反应,又能发生聚合反应的是
查看答案和解析>>
科目:高中化学 来源: 题型:
从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O===7X+5FeSO4+12H2SO4,下列说法正确的是 ( )
A.X的化学式为CuS,它既是氧化产物又是还原产物
B.5 mol FeS2发生反应,有10 mol电子转移
C.产物中的SO 有一部分是氧化产物
有一部分是氧化产物
D.FeS2只作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计如下图所示原电池(盐桥中装有含琼胶的KCl饱和溶液)。
该电池工作时,下列说法正确的是
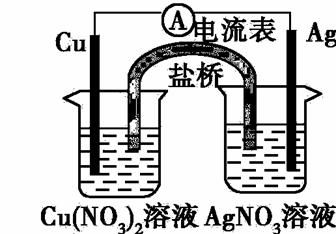
A.盐桥中的K+ 移向AgNO3溶液
B.负极反应为:Ag –e— =Ag+
C.该装置可将电能转化为化学能
D.在外电路中,电子由银电极流向铜电极
查看答案和解析>>
科目:高中化学 来源: 题型:
在体积不变的密闭容器中,2A(g)+2B(g) 3C(g)+D(g)达到平衡状态的标志是.
3C(g)+D(g)达到平衡状态的标志是.
A.单位时间内生成2n mol A,同时生成n mol D
B.容器内压强不随时间而变化
C.单位时间内生成n mol B,同时消耗1.5n mol C
D.容器内混合气体密度不随时间而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中各微粒浓度关系判定不正确的是
A.10mL 0.2 mol·L-1的氨水与l0mL 0.1 mol·L-1的盐酸充分反应混合后的溶液中,存在
c(NH4+)+c(NH3·H2O)=2c(Cl-)= 0.1 mol·L-1
B.已知酸性HF > CH3COOH,物质的量浓度相等的NaF与CH3COOK溶液中:
c(Na+) - c(F-) > c(K+) - c(CH3COO-)
C.CH3COOK溶液中加入少量NaNO3固体后的碱性溶液一定有:
c(K+) + c(H+) = c(CH3COO-) + c(OH-)
D.NaHSO3溶液中一定有:c(Na+)> c(HSO3-)> c(SO32-)>c(H2SO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
高分子化合物G是作为锂电池中 Li+ 迁移的介质,合成G的流程如下:
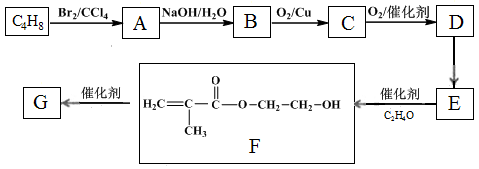
已知:①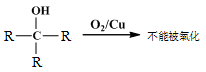
②
(1)D的官能团名称是 。
(2)A→B的反应类型是 。
(3)C的结构简式是 。
(4)D→E反应条件是 。
(5)G的结构简式是 。
(6)已知:
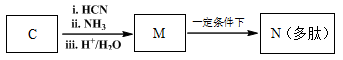
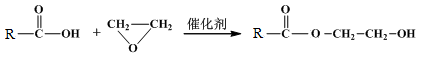
M→N的化学方程式是 。
(7)D的同分异构体中,写出有顺反异构的结构简式
注意:①两个羟基连在同一个碳上,羟基连在双键的碳上的结构不稳定都不予考虑。
②不考虑过氧键和环状结构 ③顺反结构均写出
查看答案和解析>>
科目:高中化学 来源: 题型:
某金属晶体M有两种堆积形式,如下图甲和乙,在T℃以上时甲可以转变为乙,这两种结构中最邻近的原子间距离相同。

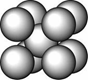
甲 乙
(1)乙的堆积方式称为 堆积;
甲和乙两种堆积方式中配位数之比为 ,晶胞边长之比为 。
(2)在T℃以下测定该金属晶体有关性质参数如下表所示。已知原子化热指1mol金属由固态转变为气态原子时所需要吸收的热量,是衡量金属键强弱的物理量。
| 金属 | 相对原子质量 | 密度/g·㎝-3 | 原子化热/kJ·mol-1 |
| Na | 22. 99 | 0. 960 | 108. 4 |
| M | 60. 20 | 7. 407 | 7735 |
预测该金属的熔点比Na (填“高”或“低”),由上述数据可计算M原子的原子半径为 pm。
(已知 ,7. 407≈
,7. 407≈ ,1pm=10
,1pm=10 m)
m)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com