
分析 (1)设氢气为xmol,则丙烷为(1-x)mol,热化学方程式中物质的量与热量成正比,结合混合气体1mol完全燃烧生成液态水时放热1252.5kJ计算;
(2)由①C3H8(g)+5O2(g)═3CO2(g)+4H2O(1)△H=-2220.0kJ/mol
②H2O(1)=H2O(g)△H=+44.0kJ/mol,
结合盖斯定律可知,①+②×4得到C3H8(g)+5O2(g)=3CO2(g)+4H2O(g),以此来解答.
解答 解:(1)设氢气为xmol,则丙烷为(1-x)mol,
H2和C3H8的混合气体共1mol,完全燃烧生成液态水时放热1252.5kJ,则
570x+(1-x)×2220=1252.5,
解得x=0.5mol,
则混合气体中H2和C3H8的体积比是0.5mol×Vm:(1mol-0.5mol)×Vm=1:1,
故答案为:1:1;
(2)由①C3H8(g)+5O2(g)═3CO2(g)+4H2O(1)△H=-2220.0kJ/mol
②H2O(1)=H2O(g)△H=+44.0kJ/mol,
结合盖斯定律可知,①+②×4得到C3H8(g)+5O2(g)=3CO2(g)+4H2O(g),△H=(-2220.0kJ/mol)+(+44.0kJ/mol)×4=-2044KJ/mol,
即丙烷燃烧生成CO2和气态水的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(g)△H=-2044KJ/mol,
故答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(g)△H=-2044KJ/mol.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、焓变及热量的计算等为解答的关键,侧重分析与应用能力的考查,注意盖斯定律的应用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为黄色 | 2Fe2++Cl2=2Fe3++2Cl- | Fe2+具有还原性 |
| ② | 在FeCl2溶液中加入锌片 | (不写) | Zn+Fe2+=Zn2++Fe | Fe2+具有氧化性 |
| ③ | 在FeCl3溶液中加入足量铁粉 | 溶液由黄色变为浅绿色 | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 |
| ④ | 在FeCl3溶液中滴入适量KI溶液和淀粉溶液 | 变蓝色 | 2Fe3++2I-=2Fe2++I2 | Fe3+具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
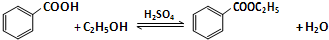
| 物质 | 颜色状态 | 密度/g/cm3 | 熔点/℃ | 沸点/℃ |
| 苯甲酸 | 白色固体 | 1.2659 | 122 | 249 |
| 苯甲酸乙酯 | 无色液体 | 1.05 | -34.6 | 212.6 |
| 乙酸 | 无色液体 | 1.0492 | 16.6 | 117.9 |
| 乙醇 | 无色液体 | 0.789 | -117.3 | 78.5 |
| 乙酸乙酯 | 无色液体 | 0.894-0.898 | -83.6 | 77.1 |
| 乙醚 | 无色液体 | 0.713 | -116.3 | 34.6 |
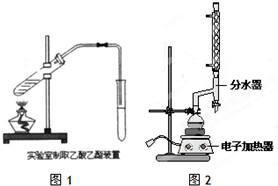
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
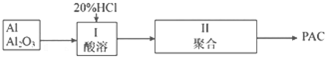
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
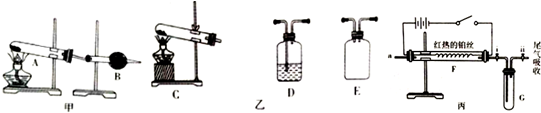
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
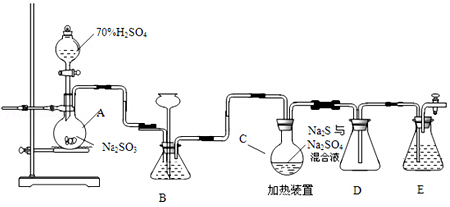
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.5 L该溶液中钠离子的物质的量浓度为0.1 mol/L | |
| B. | 1 L该溶液中含有Na2CO3的质量为10.6 g | |
| C. | 从1 L该溶液中取出100 mL,则取出溶液中Na2CO3的物质的量浓度为0.01 mol/L | |
| D. | 取该溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,将22.4 L HC1溶于1L水,可配成1 mol•L-l的稀盐酸 | |
| B. | 将100 mL 18 mol•L-1的浓H2SO4和100 mL水混合,可配成9 moI•L-l的H2SO4溶液 | |
| C. | 将4.0 g NaOH溶于100 mL容量瓶中,加水至刻度线,配成1 mol•L-1的NaOH溶液 | |
| D. | 将0.1 mol NaCl配成100 mL溶液,从中取出10 mL,所取出溶液的物质的量浓度为1 mol•L-l |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com