
【题目】氮、磷、砷为同主族元素,回答下列问题:
(1)基态As原子的核外电子排布式为___________________。
(2)稼氮砷合金材料的太阳能电池效率达40%,Ga、N、As电负性由大至小的顺序是__________________
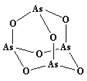
(3)As4O6的分子结构如右图所示,其中As原子的杂化方式为___________________,1 mol As4O6含有σ键的物质的量为_______________。
(4)该族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如右图所示。则Y轴可表示的氢化物(RH3)性质可能是 。
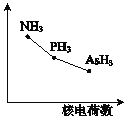
A.稳定性 | B.沸点 | C.R-H键能 | D.分子间作用力 |
(5)AsH3的沸点(-62.5℃)比NH3的沸点(-33.5℃)低,原因是
【答案】(1)[Ar]3d104s24p3;
(2)N>As>Ga;
(3)sp3 ;12mol;
(4)ac;
(5)NH3分子间能形成氢键,而As的原子半径比N的大,电负性比N的小,AsH3分子间不能形成氢键;
【解析】试题分析:(1)As为35号元素,基态As原子的核外电子排布式为[Ar]3d104s24p3,故答案为:[Ar]3d104s24p3;
(2)元素的非金属性越强,电负性越大,Ga和As同周期,Ga<As,N和As同主族,N>As,电负性由大至小的顺序是N>As>Ga,故答案为:N>As>Ga;
(3)As4O6的分子中As原子形成3个As-O键,含有1对孤对电子,杂化轨道数目为4,杂化类型为sp3杂化,根据As4O6的分子结构,1 mol As4O6含有σ键的物质的量为12mol,故答案为:sp3 ;12mol;
(4)A.N、P、As位于周期表同一主族,从上到下排列,根据元素周期律可知,非金属性越强,氢化物的稳定性越强,因此三种氢化物的稳定性逐渐降低,A正确;B.由于氨气分子间存在氢键,因此氨气的沸点最高,AsH3的相对分子质量大于PH3,AsH3沸点较高,故B错误;C.非金属性越强与氢元素形成的共价键越强,键能越大,因此R-H键能随原子序数的增大而减小,故C正确;D.三种氢化物生成的晶体均是分子晶体,分子间作用力随相对分子质量的增加而增大,故D错误;故答案为:AC;
(5)NH3分子间能形成氢键,而As的原子半径比N的大,电负性比N的小,AsH3分子间不能形成氢键,使得AsH3的沸点(-62.5℃)比NH3的沸点(-33.5℃)低,故答案为:NH3分子间能形成氢键,而As的原子半径比N的大,电负性比N的小,AsH3分子间不能形成氢键。


科目:高中化学 来源: 题型:
【题目】下列各组中的两种物质作用时,反应条件(反应温度和反应物用量)改变, 不会引起产物种类变化的是( )
A. Ca(OH)2和CO2 B. Fe和HCl
C. Na和O2 D. C和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说话正确的是( )
A.构成单质分子的粒子一定含共价键
B.非金属元素组成的化合物一定不是离子化合物
C.第ⅠA族和第ⅦA族原子化合时一定形成离子键
D.共价化合物中一定不含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
![]()
(1)A、B、C三种元素的名称分别为________、________、________。
(2)B位于元素周期表中第________周期,第________族。
(3)C的单质与H2反应的化学方程式为_________
(4)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用已知物质的量浓度为0.100 0 mol·L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化,如何判断滴定终点: 。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 (填序号)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
(3)若第一次滴定开始和结束时,酸式滴定管中的液面如下图所示。则起始读数为V1= mL,终点读数V2= mL。
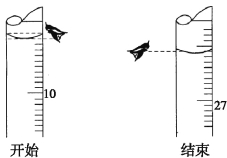
(4)再结合下表数据,计算被测氢氧化钠溶液的物质的量浓度是 mol·L-1。
滴定次数 | 待测溶液体积/mL | 标准酸体积 | |
滴定前的刻度/mL | 滴定后的刻度/mL | ||
第一次 | 10.00 | V1 | V2 |
第二次 | 10.00 | 4.10 | 21.10 |
第三次 | 10.00 | 0.40 | 17.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖原[(C6H10O5)n]是一种相对分子质量比淀粉更大的多糖,主要存在于肝脏中,所以又叫动物淀粉和肝糖。下列关于糖原的叙述正确的是( )
A. 糖原与淀粉、纤维素互为同分异构体 B. 糖原、淀粉、纤维素属于同系物
C. 糖原水解的最终产物是葡萄糖 D. 糖原具有还原性,能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com