
| V |
| Vm |
| m |
| n |
| 0.448L |
| 22.4L/mol |
| m |
| n |
| V |
| Vm |
| m |
| n |
| m | ||
|
| mVm |
| V |
| mVm |
| V |
| 0.448L |
| 22.4L/mol |
| m |
| n |
| 1.28g |
| 0.02mol |


科目:高中化学 来源: 题型:
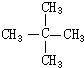 b.CH3CH2CH2CH2CH3 c.CH3CH=CHCH3 d.CH3CH=CH2
b.CH3CH2CH2CH2CH3 c.CH3CH=CHCH3 d.CH3CH=CH2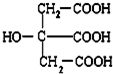
查看答案和解析>>
科目:高中化学 来源: 题型:
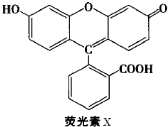
| A、1molX与足量的NaOH溶液在常温常压下反应,最多消耗3molNaOH |
| B、1molX最多能与9mol氢气反应 |
| C、X与足量的浓溴水反应,最多消耗4molBr2 |
D、X能与糠醛(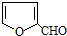 )发生缩聚反应 )发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 浓度相同的NaOH溶液各100mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得的溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸的体积之间的关系如图所示,下列判断正确的是( )
浓度相同的NaOH溶液各100mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得的溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸的体积之间的关系如图所示,下列判断正确的是( )| A、通入CO2后,不能确定A烧杯中的溶质 |
| B、B烧杯中通入的CO2体积为448mL |
| C、原NaOH溶液的浓度为0.2mol/L |
| D、通入CO2后,C烧杯中溶质成分为NaOH和Na2CO3,且物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
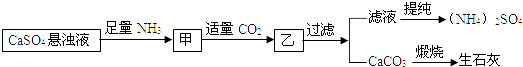
| A、生成lmol(NH4)2SO4至少消耗2molNH3 |
| B、上述反应过程中发生了氧化还原反应 |
| C、反应的离子方程式为:Ca2++2NH3+CO2+H2O═CaCO3↓+2NH4+ |
| D、直接蒸干滤液得到纯净的(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com