
【题目】物质X的结构简式如图所示,它常用于制香料或作为饮料酸化剂,在医学上也有广泛用途。下列关于物质X的说法正确的是( )
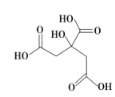
A.X的分子式为C6H7O7
B.X分子内所有原子均在同一平面内
C.1mol物质X最多可以和3mol氢气发生加成反应
D.足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体的物质的量相同
科目:高中化学 来源: 题型:
【题目】利用铝热炼镁还原渣[Al、Ca(AlO2)2、Al2O3、MgO及少量不能被碱液溶出的尖晶石型铝的化合物等]制取Al(OH)3的工艺流程如下:
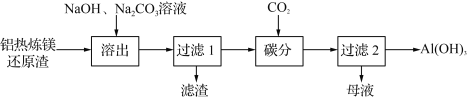
(1) “滤渣”成分包括:水合铝酸钙、尖晶石型铝的化合物、不含铝的化合物______________(写两种物质的化学式)。
(2) “溶出”时,在适当条件下,铝及其大部分含铝化合物以NaAlO2溶出。
①金属Al与NaOH溶液反应的化学方程式为________________________________。
②其他条件相同时,Na2CO3、NaOH溶液的浓度对铝的溶出率的影响如图所示:
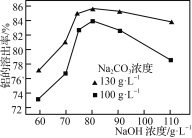
NaOH溶液浓度一定时,130 g·L-1的Na2CO3溶液对铝的溶出率比100 g·L-1的大,这是因为______________(从平衡移动角度分析);Na2CO3溶液浓度一定时,当NaOH溶液浓度大于80 g·L-1,铝的溶出率随NaOH溶液浓度增大而减小,可能原因是______________。
(3) “碳分”时,溶液与过量CO2反应的离子方程式为________________________。
(4) “过滤2”的母液经再生处理可返回“溶出”工序循环使用,再生的方法是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油的成分之一,它的结构简式为: ![]() ,请回答:
,请回答:
(1)胡椒酚所含官能团的名称为____。
(2)它能发生的化学反应是___(填序号)。
①氧化反应 ② 取代反应 ③ 加成反应 ④消去反应 ⑤ 加聚反应
(3)1 mol 胡椒酚与氢气发生加成反应,理论上最多消耗____ mol H2。
(4)1 mol 胡椒酚与浓溴水发生反应,理论上最多消耗_____mol Br2。
(5)若要制备胡椒酚钠,可以选择的试剂是____(填序号)。
① Na ② NaOH ③ NaHCO3 ④ Na2CO3
(6)写出所有符合下列条件的胡椒酚的同分异构体的结构简式:____。
① 能发生银镜反应;② 苯环上有两个取代基,且苯环上的一氯代物有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 a~g 在表中的位置如右表,请回答下列问题:

(1)d、e元素常见离子的半径由大到小的顺序为(用化学式表示)__________;b、c两元素非金属性较强的是(写元素符号)_________,写出能证明这一结论的一个化学方程式_____________。
(2)下列有关说法正确的是(___)
A.e在 d2 中燃烧,生成e2d
B.加热熔化eda时不可用Al2O3坩埚,可用瓷坩埚
C.将 gd2 通入溴水中,溴水褪色,体现了gd2 的漂白性
D.将打磨过的 f 置于酒精灯上点燃,观察到f 熔化但未见液滴滴落
(3)上述元素可组成盐 R:ca4f(gd4)2和盐S:ca4agd4。
①相同条件下,0.1 mol·L-1盐R中 c(ca4+) _______(填“=”、 “>”或“<”)0.1 mol·L-1盐S中c(ca4+)。
②R常用作净水剂,其原理为(用离子方程式表示)______________。
③向盛有 10 mL 1 mol·L-1盐S溶液的烧杯中滴加1 mol·L-1 NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是_____________。
④向盛有 10 mL 1 mol·L-1盐R溶液的烧杯中滴加 1 mol·L-1NaOH溶液 32 mL后,继续滴加至35 mL,写出此时段(32 mL~35 mL)间发生的离子方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答以下问题:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是__________________________。
(2)另称取已去除表面氧化物的铁钉(碳素钢)6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。写出生成Fe2+所有可能的离子方程式:______________。
②乙同学取336mL(标准状况)气体Y通入足量氯水中,发生反应的化学方程式为:______________。
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为___________。
(3)向100mL水中投入Na和Al共16克,充分反应后剩余金属1g。计算放出H2的体积为________升(标准状况下)
(4)向含有0.3mol NaAlO2的溶液中滴加1mol/L HCl,当生成7.8克沉淀时,加入盐酸的体积为________mL
(5)向一定量的Fe、Fe2O3和CuO混合物投入120 ml 2.2 mol/L的硫酸溶液中,充分反应后生成896 mL标准状况下的气体,得不溶物1.28 g,过滤后,向滤液中加入2 mol/L的NaOH溶液,加至40 mL时开始出现沉淀,则滤液中FeSO4的物质的量浓度为(设滤液体积为120 ml)_________mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物瑞德西韦(Remdesivir)对新冠病毒有明显抑制作用,化合物 M是合成瑞德西韦的中间体,下列关于M的说法错误的是
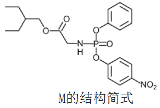
A.核磁共振氢谱共有11个吸收峰
B.分子中含有3种含氧官能团
C.分子中N原子一个是sp2杂化,一个是sp3杂化
D.1mol该物质与足量NaOH溶液反应时消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烷烃和某气态单烯烃(只含一个碳碳双键)组成的混合气体在同温、同压下是氢气密度的13倍,取标准状况下此混合气体4.48L,通入足量溴水中,溴水质量增加2.8g,则此混合气体可能是( )
A.甲烷和丙烯B.乙烷和丙烯
C.甲烷和2-甲基丙烯D.乙烷和1-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的说法中
①结构片段为…… ……的高聚物,其单体是甲醛和苯酚
……的高聚物,其单体是甲醛和苯酚
②标准状况下,22.4LHF所含电子数约为10NA
③甲醇通常是一种有毒的气体,分子中只含极性键
④苯酚和碳酸钠溶液的反应:![]()
⑤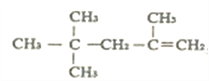 的名称为:2,4,4,-三甲基-1-戊烯
的名称为:2,4,4,-三甲基-1-戊烯
⑥3-甲基-1-丁烯中的所有碳原子不可能处于同一平面
⑦等物质的量的苯与苯甲酸完全燃烧消耗氧气的量不相等
其中正确的有 个。
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白皮杉醇具有抗炎、抗菌、抗氧化、抗白血病、提高免疫调节功能等功效,其人工合成过程涉及了如下转化:
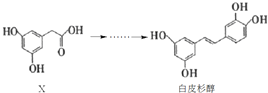
下列说法正确的是
A.X的分子式为C8H10O4
B.化合物X、白皮杉醇均可与Na2CO3溶液反应并放出气体
C.白皮杉醇与浓溴水反应时,最多可消耗6molBr2
D.在一定条件下,白皮杉醇可发生加成、取代、氧化和聚合反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com