
【题目】在2L密闭容器中,发生3A(g)+B(g)2C(g)的反应,若最初加入A和B都是4mol,A的平均反应速率为0.12molL﹣1s﹣1 , 则10s后容器中B的物质的量是( )
A.1.6 mol
B.2.8 mol
C.3.2 mol
D.3.6 mol
【答案】C
【解析】A的平均反应速率为0.12molL﹣1s﹣1 , 则v(B)= ![]() ×0.12molL﹣1s﹣1=0.04molL﹣1s﹣1 ,
×0.12molL﹣1s﹣1=0.04molL﹣1s﹣1 ,
故10s后容器中B的物质的量浓度= ![]() ﹣0.04molL﹣1s﹣1×10s=1.6 mol/L,
﹣0.04molL﹣1s﹣1×10s=1.6 mol/L,
B物质的量=1.6 mol/L×2L=3.2mol,故选C。
【考点精析】认真审题,首先需要了解化学反应速率的概念(化学反应速率是用来衡量化学反应进行快慢程度的,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示),还要掌握化学平衡的计算(反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%)的相关知识才是答题的关键.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含有氯气的气体经过甲瓶后,通入乙瓶 ,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色。甲瓶中所盛的试剂可能是( )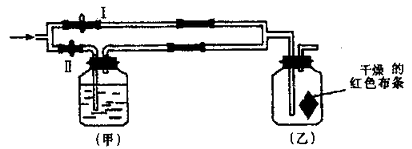
①浓H2SO4 ②浓NaOH溶液 ③KI溶液 ④饱和NaCl溶液
A.②
B.②③
C.①②③
D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应是化学反应中的基本反应之一,研究氧化还原反应,对人类的进步具有极其重要的意义.
(1)已知:2BrO3﹣+C12═Br2+2C1O3﹣; 5C12+I2+6H2O═2HIO3+10HC1;C1O3﹣+5C1﹣+6H+═3C12+3H2O则C1O3﹣、BrO3﹣、IO3﹣、C12的氧化性由弱到强的排序为
(2)已知Fe3+的氧化性强于I2 , 请你从所给试剂中选择所需试剂,设计一个实验加以证明.(提示:请写出实验步骤、现象及结论)①FeCl3溶液 ②碘水 ③KI溶液 ④稀H2SO4 ⑤淀粉溶液
(3)二十世纪初期,化学家合成出极易溶于水的NaBH4 . 在强碱性条件下,常用NaBH4处理含Au3+的废液生成单质Au,已知,反应后硼元素以BO2﹣形式存在,反应前后硼元素化合价不变,且无气体生成,则发生反应的离子方程式为
(4)某强氧化剂[RO(OH)2]+能将Na2SO3氧化.已知含2.0×10﹣3mol[RO(OH)2]+离子的溶液,恰好跟25.0mL 0.2mol/L 的Na2SO3溶液完全反应,则反应后R的化合价为价.
(5)将32g 铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.请回答:
①待产生的气体全部释放后,向溶液加入V mL amolL﹣1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为mol/L.(用含V、a的式子表示)
②欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3 , 至少需要H202的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2 , 而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。 
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应:2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)装置①中发生反应的离子方程式是;
(2)装置②的目的是 , 发生反应的化学方程式是;
(3)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是 ;
(4)实验的具体操作是:先检验装置的气密性,再加入药品,然后(此操作的目的是),最后滴加浓硝酸;
(5)该小组得出的结论所依据的实验现象是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近我国科研人员根据玉兔二号在第一个月昼的光谱探测数据,分析得出月幔中富含橄榄石(主要成分为:(MgFe)2SiO4),橄榄石属于
A. 碱B. 酸C. 硅酸盐D. 酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.1mol FeI2与足量氯气反应时转移的电子数为2NA
B.常温常压下,46gNO2和N2O4混合气体含有的原子数为3NA
C.1molCl2参加的氧化还原反应,反应过程中转移电子数都是2NA
D.56g铁片投入足量浓H2SO4中生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食物中碲的一个来源是装食物的含锡罐头。通常开罐时约有8毫克金属屑落入食物中,其中含碲0.1%(即8微克)。因此,用塑料包装代替罐头可以防止摄入碲,碲具有内在的毒性,碲可能会包含在酶体系 中,与蛋白配合,引起肾和肝退化。碲在元素周期表中的位置是( )
A.第四周期IVA族B.第五周期IVA族C.第四周期VIA族D.第五周期VIA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com