下列叙述正确的是( )
A.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl)
B.0.1mol?L-1的CH3COOH溶液加水稀释,溶液中c(OH-)减小
C.0.2mol?L-1HCl溶液与等体积0.05mol?L-1Ba(OH)2溶液混合后,溶液的pH=1
D.0.2mol?L-1的NaHCO3溶液中c(H+)+c(H2CO3)=2c(CO32-)+c(OH-)
【答案】
分析:A、比较不同溶液中c(NH
4+),需要考虑其他离子对NH
4+水解的影响;
B、CH
3COOH溶液加水稀释,酸性减弱,c(H
+)减小,c(OH
-)会随c(H
+)减小而变大;
C、酸碱溶液混合后溶液的pH值的计算,首先要判断是酸还是碱剩余,再根据剩余的c(H
+)或c(OH
-)求pH值;
D、NaHCO
3溶液中存在水解也存在电离,存在着电荷、物料和质子守恒.
解答:解:A、如果没有水解,c(NH
4Cl)应该是c[(NH
4)
2Fe(SO
4)
2]、c[(NH
4)
2SO
4]的2倍,由于水解程度比较小,因此c(NH
4Cl)应是最大的.(NH
4)
2Fe(SO
4)
2中NH
4+和Fe
2+都水解呈酸性,水解相互抑制,因此(NH
4)
2Fe(SO
4)
2中NH
4+的水解程度(NH
4)
2SO
4的要小,c[(NH
4)
2Fe(SO
4)
2]比c[(NH
4)
2SO
4]的小,故A正确;
B、在溶液中,c(H
+)?c(OH
-)=K
W,c(H
+)减小,c(OH
-)变大,故B错误;
C、由题可知,混合后盐酸有剩余,c(H
+)=
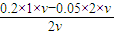
=0.05mol/L,pH=-lg(0.05)=2-lg5,故C错误;
D、HCO
3-在溶液中能发生水解:HCO
3-+H
2O?H
2CO
3 +OH
-),也能发生电离:HCO
3-?CO
32-+H
+;
电荷守恒:c(H
+)+c(Na
+)=2c(CO
32-)+c(OH
-)+c(HCO
3-);
物料守恒:c(Na
+)=c(CO
32-)+c(H
2CO
3 )+c(HCO
3-);将电荷守恒和物料守恒合并消去c(Na
+)
得到c(H
+)+c(H
2CO
3)=c(CO
32-)+c(OH
-),故D错误.
故选A.
点评:本题主要考查了离子浓度大小的比较,能熟练写出电荷守恒、物料守恒和质子守恒.做这一部分题要细心.

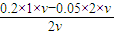 =0.05mol/L,pH=-lg(0.05)=2-lg5,故C错误;
=0.05mol/L,pH=-lg(0.05)=2-lg5,故C错误;
